![]() Амилоидоз
Амилоидоз – системное заболевание, характеризующееся нарушением белкового обмена и функционирования иммунной системы. В результате данных нарушений образуется специфический белково-сахаридный комплекс амилоид, который откладывается практически во всех тканях организма. По мере прогрессирования заболевания амилоид вытесняет нормальные клетки из пораженного органа, обуславливая развитие необратимых изменений и утрату функциональной активности. При длительном течении заболевания и в отсутствии лечения развивается полиорганная недостаточность (
нарушение функции множества органов) и наступает смерть.
По данным последних исследований амилоидозом страдает менее 1% населения Земли, при этом частота выявления отдельных форм заболевания неодинакова. Встречаемость вторичного амилоидоза в несколько раз превышает остальные формы. Наследственный (
генетически обусловленный) амилоидоз преобладает в странах Средиземноморского бассейна, а также среди людей армянской и еврейской национальности.
Из клинических форм амилоидоза наиболее часто встречается нефропатическая (
с преимущественным поражением почек) и генерализованная форма, при которой амилоид откладывается во всех органах и тканях. Мужчины болеют почти в 2 раза чаще женщин.
Интересные факты - Химическая структура амилоида различна при разных формах патологии. Амилоидозом, по сути, называется группа заболеваний, схожих по механизму развития, клиническим и патологоанатомическим проявлениям.
- На сегодняшний день не существует методов лечения, позволяющих раз и навсегда избавиться от амилоидоза.
- Амилоидоз может развиваться на протяжении десятилетий, при этом никак себя не проявляя.
- Причины некоторых форм амилоидоза науке неизвестны.
Что такое амилоид?
![]()
Амилоидоз относится к диспротеинозам, то есть к болезням, протекающим с нарушением белкового обмена. В то же время доказано, что данное заболевание развивается лишь при нарушении функционирования иммунной системы, поэтому для понимания сути патологических процессов, происходящих в организме больного, необходимы определенные знания из области иммунологии и физиологии.
Строение и функции иммунной системы
Иммунная система человека представляет собой комплекс органов и клеток (
лейкоцитов), участвующих в защите организма от воздействия чужеродных микроорганизмов (
бактерий, вирусов, грибов и других) и собственных клеток, представляющих опасность для человека (
например, опухолевых клеток или «старых» клеток крови).
Основными органами иммунной системы являются: - Красный костный мозг. Особый тип ткани, располагающийся в полостях костей (таза, тел позвонков, грудины и других) и участвующий в образовании всех клеток крови.
- Тимус (вилочковая железа). Данный орган располагается в грудной клетке. В нем происходит размножение и дифференцировка («обучение») некоторых клеток иммунной системы (Т-лимфоцитов).
- Лимфатические узлы. Данные образования располагаются по ходу кровеносных сосудов во всех органах и тканях. Они содержат большое количество иммунных клеток (лимфоцитов) и представляют собой барьер, предотвращающий распространение чужеродных бактерий и вирусов из очага инфекции по всему организму.
- Селезенка. В селезенке происходят процессы дифференцировки лимфоцитов, а также разрушаются фрагменты чужеродных микроорганизмов и старых или поврежденных клеток крови.
- Пейеровы бляшки. Данным термином обозначаются небольшие (диаметром несколько миллиметров) скопления лимфоидной ткани, располагающиеся в стенках кишечника.
Основными клетками иммунной системы являются: Лимфоциты Данные клетки не только принимают непосредственное участие в защите организма, но и регулируют деятельность всей иммунной системы.
По функциональным признакам различают: - В-лимфоциты. Любой чужеродный микроорганизм имеет на своей поверхности различные структурные компоненты, называемые антигенами. При контакте с «чужим» антигеном В-лимфоциты превращаются в так называемые плазмоциты, которые начинают вырабатывать специфические антитела (иммуноглобулины класса A, G, M, D и E). Иммуноглобулин представляет собой гликопротеид (белково-сахаридный комплекс), состоящий из белка и связанных с ним сахаридов (глюкозы, фруктозы и других). Данные антитела взаимодействуют только с тем антигеном, против которого они были выработаны, вызывая его уничтожение и гибель клетки, на которой он расположен.
- Т-лимфоциты. Способны обнаруживать и уничтожать клетки, пораженные вирусами, а также опухолевые клетки (данную функцию выполняют так называемые Т-киллеры). Другие разновидности Т-лимфоцитов участвуют в регуляции иммунного ответа организма. Одни из них (Т-хелперы) усиливают активность В-лимфоцитов, стимулируя образование большего количества антител, в то время как другие (Т-супрессоры) оказывают угнетающее влияние на активность всех остальных лимфоцитов.
- NK-клетки. Обеспечивают противоопухолевую и противовирусную защиту организма.
Моноциты Моноцитами называются крупные клетки иммунной системы, которые циркулируют в крови в течение 2 – 3 дней, после чего переходят в ткани организма, превращаясь в так называемые гистиоциты. Гистиоциты поглощают и разрушают попавшие в ткань чужеродные антигены, а также собственные поврежденные лейкоциты.
Базофилы, нейтрофилы и эозинофилы Являясь разновидностями лейкоцитов, данные клетки также участвуют в защите организма от чужеродных бактерий, внутриклеточных и внеклеточных паразитов и опухолевых клеток.
Система макрофагов
Макрофагами называются особые крупные клетки, которые образуются в процессе эмбрионального развития во всех тканях человеческого организма, а также поступают в ткани из крови в течение жизни человека. Данные клетки обладают способностью поглощать (
фагоцитировать) и разрушать чужеродные микроорганизмы, фрагменты погибших клеток и других микрочастиц, попавших в ткань.
Основными макрофагами человеческого организма являются: - моноциты крови;
- гистиоциты;
- макрофаги печени (Купферовские клетки);
- легочные макрофаги;
- эндотелиальные клетки (эндотелий – внутренняя поверхность сосудов) селезенки, лимфатических узлов, костного мозга.
При попадании инфекции в организм происходит активация клеток системы макрофагов и их усиленное размножение, в результате чего обеспечивается защита органов и тканей от повреждающего действия чужеродных микроорганизмов и их
токсинов.
Механизм образования амилоида
Как говорилось ранее, термином «амилоидоз» объединяется группа схожих заболеваний, общим для которых является накопление амилоида в тканях организма. Амилоид представляет собой сложный комплекс, который на 95% состоит из специфического фибриллярного белка и на 5% из нуклеопротеидов (
белково-сахаридных комплексов) крови и тканей. Фибриллярный белок в норме в организме не встречается и образуется только при развитии амилоидоза.
Образование амилоида характеризуется: - Образованием амилоидобластов. Первый этап развития амилоидоза характеризуется мутационными изменениями, происходящими в различных клетках иммунной системы. Клетки системы макрофагов, моноциты, лимфоциты и некоторые другие мутируют, превращаясь в качественно новый тип клеток – амилоидобласты. По мере прогрессирования заболевания количество амилоидобластов увеличивается, и они заселяют различные органы (селезенку, печень, костный мозг, лимфатические узлы и другие).
- Синтезом фибриллярного белка. Внутри амилоидобластов образуется фибриллярный белок, представляющий собой тонкие и длинные структуры (нити), которые впоследствии объединяются, формируя так называемый каркас амилоида. Фибриллярный белок является чужеродным для организма, поэтому в ответ на его появление запускаются характерные защитные реакции. Вокруг амилоидобластов появляются другие клетки, которые поглощают и разрушают выделяющийся из амилоидобластов фибриллярный белок, препятствуя его поступлению в ткани организма. Данный процесс может длиться неопределенно долгий промежуток времени (так называемая латентная, скрытая стадия заболевания), однако в конечном итоге всегда развивается иммунологическая толерантность (то есть организм «привыкает» к новому белку и перестает «защищаться» от него), в результате чего большое количество фибриллярного белка поступает в ткани.
- Отложением амилоида в тканях. Образование амилоида происходит в межклеточном пространстве в результате соединения фибриллярного белка с различными белками и нуклеопротеидами крови и тканей. Связь, образующаяся между данными веществами, настолько прочная, что разрушить ее практически невозможно, в результате чего образующийся амилоид накапливается в тканях, постепенно вытесняя нормальные клетки органа.
При некоторых формах амилоидоза в амилоидобласты могут превращаться и клетки других органов, что будет обуславливать клинические проявления заболевания.
В амилоидобласты могут превращаться: - Кардиомиоциты (мышечные клетки сердца) – при амилоидозе сердца.
- Кератиноциты – при амилоидозе кожи.
- Гладкие мышечные клетки – при амилоидозе крупных кровеносных сосудов.
- В-клетки поджелудочной железы (продуцирующие инсулин) – при инсулярном амилоидозе.
- С-клетки щитовидной железы (секретирующий гормон кальцитонин).
- Клетки APUD-системы – представляют собой рассеянные по всему организму клетки, продуцирующие различные типы гормонов.
Стоит отметить, что описанный механизм характерен для большинства, но не для всех видов амилоидоза. В некоторых случаях образование амилоида происходит по другим механизмам, которые на сегодняшний день окончательно не изучены.
Типы амилоида
Амилоид, образующийся при различных видах заболевания, структурно неодинаков. В зависимости от состава и строения выделяют несколько типов амилоида (
более 15), механизмы образования которых также различны.
Двумя основными типами амилоида являются: - АА-амилоид. При развитии любого воспалительного процесса запускается целый ряд биохимических реакций, в том числе происходит синтез и выделение в кровоток так называемых белков острой фазы воспаления, одним из которых является сывороточный белок амилоида А (SAA). В норме он циркулирует в крови непродолжительное время и потом разрушается. При хронических воспалительных заболеваниях концентрация белка SAA в плазме поддерживается на высоком уровне в течение длительного времени. В результате его неполного расщепления и образуется фибриллярный компонент АА-амилоида.
- AL-амилоид. Фибриллярные белки AL-типа выделяются из амилоидобластов (мутировавших плазмоцитов) и представляют собой аномальные цепи иммуноглобулинов.
Другие типы амилоида (
AF, AH, AE и так далее) образуются при конкретных формах амилоидоза.
Причины амилоидоза
![]()
Амилоидоз может являться самостоятельным заболеванием либо развиться в результате патологии других органов и систем.
В зависимости от причины развития различают: - первичный (идиопатический) амилоидоз;
- вторичный (реактивный) амилоидоз;
- наследственный амилоидоз;
- старческий амилоидоз;
- амилоидоз при опухолях;
- амилоидоз у пациентов на гемодиализе.
Первичный амилоидоз
Данная форма заболевания характеризуется отложением амилоида во многих органах и тканях, причем причину его образования установить, как правило, не удается. В абсолютном большинстве случаев при первичном амилоидозе отмечается мутационное перерождение клеток иммунной системы и образование AL-амилоида, который накапливается в тканях мезодермального происхождения (
в сердечно-сосудистой системе, мышцах, нервах и коже).
Другой причиной образования AL-амилоида может быть
миеломная болезнь (плазмоцитома) – опухолевое заболевание, характеризующееся злокачественным перерождением и размножением плазмоцитов (
дифференцированных В-лимфоцитов). Они выделяют аномальные глобулины в больших количествах, которые связываются с нуклеопротеидами плазмы и превращаются в амилоид.
Вторичный амилоидоз
Вторичный амилоидоз характеризуется образованием АА-амилоида и развивается в результате длительно прогрессирующих воспалительных процессов, то есть всегда является осложнением других заболеваний.
Причиной вторичного амилоидоза могут быть: Вторичный амилоидоз может поражать практически любые органы и ткани в организме человека. Клиническая картина начинает проявляться через несколько лет (
иногда через десятилетия) после начала основного заболевания и характеризуется нарушением функции того органа, в котором отложение амилоида наиболее выражено (
обычно это почки и надпочечники, печень, селезенка, лимфатические узлы). По мере прогрессирования заболевания поражаются остальные органы, развивается полиорганная недостаточность и наступает смерть.
Наследственный амилоидоз
Генетический аппарат человека состоит из 23 пар
хромосом, каждая из которых содержит огромное количество генов. Каждый ген, в свою очередь, кодирует образование определенных белков в клетке, что в конечном итоге определяет ее строение и функции. Наследственные формы амилоидоза характеризуются наличием генетических мутаций в клетках иммунной системы, которые передаются из поколения в поколение и приводят к образованию амилоидобластов. Данная форма заболевания диагностируется у людей определенных этнических групп либо проживающих в определенной местности.
К наследственному амилоидозу относится: - Периодическая болезнь (семейная средиземноморская лихорадка). Данное заболевание встречается преимущественно у арабов, армян и евреев. Клинически данная форма амилоидоза характеризуется приступами лихорадки (повышением температуры выше 39ºС, проливным потом, головными и мышечными болями), сопровождающимися воспалением серозных оболочек организма – брюшины (оболочки органов брюшной полости), плевры (оболочки легких) и синовиальных оболочек (выстилающих внутренние поверхности суставов). Часто отмечаются психические отклонения.
- Семейный нефропатический амилоидоз (английский амилоидоз, болезнь Макла и Уэллса). Характеризуется приступами лихорадки, крапивницей и нарушением слуха (вплоть до глухоты).
- Наследственный нейропатический амилоидоз. Для данной формы заболевания характерно поражение нервной ткани различной локализации. Могут поражаться нервы ног (португальский амилоидоз) или рук (американский амилоидоз), а также встречается сочетанное поражение нервной системы, почек и роговицы глаза (финский амилоидоз).
- Наследственный кардиопатический амилоидоз. Встречается преимущественно у жителей Дании и по клиническим проявлениям схож с первичным генерализованным амилоидозом.
Старческий амилоидоз
У многих людей в возрасте старше 80 лет происходит отложение амилоида в различных тканях и органах. Данный процесс обычно носит локальный характер и связан с другими старческими заболеваниями.
К старческому амилоидозу относится: - Старческий церебральный (мозговой) амилоидоз. Встречается при болезни Альцгеймера и характеризуется отложением амилоида типа Ab в ткани головного мозга.
- Старческий сердечный амилоидоз. Характеризуется поражением сердечной мышцы, причем при разных формах данного заболевания образуются разные типы амилоида. Так, в состав амилоида может входить мутантная форма транстиретина (белка крови, в норме транспортирующего гормон щитовидной железы тироксин и витамин А в организме), что характеризуется преимущественным поражением желудочков сердца. В другом случае амилоид может образовываться из предсердного натрийуретического пептида (гормона, выделяющегося клетками сердца), что характеризуется отложением амилоида преимущественно в области предсердий. В обоих случаях депозиты амилоида обнаруживаются и в тканях других органов (селезенки, легких, поджелудочной железы).
Амилоидоз при опухолях
При некоторых опухолях наблюдается злокачественное перерождение клеток пораженного органа, в результате чего они начинают секретировать фибриллярный белок. Амилоидоз в данном случае носит локальный характер и характеризуется отложением амилоида в ткани органа, в котором развивается злокачественный процесс.
Причиной амилоидоза может быть: - Медуллярный рак щитовидной железы. В данном случае опухоль развивается из С-клеток щитовидной железы, которые в норме продуцируют гормон кальцитонин (регулирующий обмен кальция в организме). Образующийся при этом амилоид (AE-типа) состоит из фрагментов кальцитонина, синтез которого нарушен.
- Опухоль островков поджелудочной железы. Данные островки представляют собой скопление клеток, продуцирующих различные гормоны (инсулин, глюкагон, соматостатин и другие). При их злокачественном перерождении в окружающие ткани может выделяться фибриллярный белок, который впоследствии превращается в амилоид.
Амилоидоз у пациентов на гемодиализе
Гемодиализ (
«искусственная почка») – процесс искусственного очищения крови человека от побочных продуктов обмена веществ, которые в норме выделяются через почки. Данная процедура назначается пациентам, страдающим острой или хронической
почечной недостаточностью и заключается в пропускании крови через аппарат, содержащий особый раствор, отделенный от крови полупроницаемой мембраной. В результате этого различные вредные вещества и лишняя жидкость удаляются, а клетки крови и крупные белки возвращаются обратно в организм.
Структурной основой амилоида при длительном гемодиализе является В
2-микроглобулин (
в норме удаляющийся исключительно почками), который не фильтруется через мембрану диализатора и поэтому не выводится из организма. При хронической почечной недостаточности, когда пациенты находятся на гемодиализе в течение нескольких месяцев или лет, концентрация данного белка в крови повышается в несколько раз. Он связывается с нуклеопротеидами плазмы и выпадает в осадок в тканях различных органов (
в том числе в почках, что усугубляет почечную недостаточность).
Симптомы амилоидоза
![]()
Исходя из того, что амилоидоз может поражать практически любой орган и ткань, симптомы данного заболевания могут быть самыми разнообразными. При различных формах амилоидоза вначале отмечается преимущественное поражение одного органа, что характеризуется нарушением его функции и развитием симптомов органной недостаточности. При прогрессировании заболевания процесс распространяется по всему организму, вовлекая другие ткани. Исключение составляет локальный амилоидоз, при котором поражается лишь один орган.
Амилоидоз может проявляться: - поражением почек;
- поражением печени;
- поражением сердца;
- надпочечниковой недостаточностью;
- увеличением селезенки (спленомегалией);
- поражением желудочно-кишечного тракта (ЖКТ);
- поражением нервной системы;
- поражением кожи;
- поражением суставов;
- поражением мышц.
Поражение почек
Поражение почек является наиболее частым и в то же время наиболее опасным проявлением амилоидоза.
В клинической картине амилоидоза почек выделяют 4 стадии: - латентную (скрытую);
- протеинурическую;
- нефротическую;
- азотемическую.
Латентная стадия В латентной стадии заболевание практически никак не проявляется. При вторичных формах на первый план выступают симптомы основной патологии, а симптомы поражения почек появляются спустя несколько лет или десятилетий, однако описаны случаи более быстрого развития амилоидоза (
через 3 – 4 месяца).
Протеинурическая стадия Может длиться 10 и более лет и характеризуется отложением депозитов амилоида в почечной ткани – в мелких сосудах, в клубочках (
в которых происходит ультрафильтрация крови), в межклеточном пространстве. Все это приводит к сдавливанию, атрофии (
уменьшению в размерах) и гибели нефронов (
функциональных единиц почечной ткани, обеспечивающих образование мочи). При этом нарушается целостность почечного фильтра (
который в норме непроницаем для клеток крови и крупномолекулярных белков), в результате чего с мочой начинают выделяться белки (
протеины). Выделительная функция почек на данном этапе нарушена незначительно, поэтому заподозрить амилоидоз можно только на основании лабораторных данных.
Нефротическая стадия Дальнейшее нарушение целостности почечного фильтра приводит к развитию нефротического синдрома, характеризующегося потерей большого количества белка с мочой (
более 3 г/л) и снижением концентрации белков в крови. Так как белки участвуют в поддержании коллоидно-осмотического давления (
то есть удерживают жидкую часть крови в сосудистом русле), снижение их концентрации приводит к переходу жидкости в ткани организма, в результате чего развиваются генерализованные
отеки, являющиеся основным проявлением амилоидоза на данном этапе.
Отеки появляются независимо от положения тела и времени суток. Они начинают появляться в области лица, век, половых органов, в поясничной области. По мере прогрессирования заболевания отеки усиливаются и могут достигать крайней степени выраженности (
анасарки). Отмечается скопление жидкости в полостях организма –
асцит (
в брюшной полости), гидроторакс (
в плевральной полости), гидроперикард (
в полости сердечной сумки). Кожа становится бледной, отмечается повышенная ломкость ногтей и волос. Возможно выделение крови с мочой.
Продолжительность данной стадии обычно не превышает 4 – 6 лет, после чего (
в отсутствии лечения) развивается азотемическая стадия.
Азотемическая стадия Количество функциональной почечной ткани на данном этапе амилоидоза составляет менее 25%. Этого недостаточно, чтобы выводить из организма побочные продукты обмена веществ (
мочевину, мочевую кислоту и другие), в результате чего их концентрация в крови начинает повышаться.
Клинически почечная недостаточность проявляется: - Нарушением мочеобразования – человек может выделять менее 50 мл мочи в сутки (при норме не менее 800 мл).
- Нарушением общего самочувствия – слабостью, повышенной утомляемостью.
- Нарушением системы пищеварения – отсутствием аппетита, частой тошнотой и рвотой, сухостью во рту, неприятным запахом изо рта и так далее.
- Поражением кожных покровов – больные жалуются на кожный зуд, кожа бледная и сухая, со следами расчесов (из-за зуда).
- Поражением сердечно-сосудистой системы – может отмечаться повышение артериального давления, аритмии (нарушение частоты сердечных сокращений), гипертрофия (увеличение в размерах) сердечной мышцы.
- Повреждением мозга – развивается в результате воздействия высоких концентраций мочевины и мочевой кислоты на нервную ткань мозга и проявляется раздражительностью, бессонницей, нарушением памяти, психики и умственных способностей.
- Анемией (уменьшением концентрации гемоглобина и эритроцитов в крови) – развивается из-за недостатка эритропоэтина – вещества, синтезируемого почками и активирующего образование красных клеток крови в костном мозге.
Поражение печени
Поражение печени также является частым симптомом генерализованных форм амилоидоза. Отложения амилоида сдавливают печеночные клетки, желчевыводящие протоки и кровеносные сосуды органа, в результате чего нарушаются его функции.
При отложении депозитов амилоида в печеночной ткани отмечается увеличение размеров органа, определяемое при пальпации (
прощупывании) живота. Поверхность печени гладкая, нижний край ровный, болезненность не определяется. Стоит отметить, что даже при длительном прогрессировании амилоидоза выраженная почечная недостаточность развивается редко, что, вероятнее всего, связано высокими регенераторными (
восстановительными) способностями данного органа.
Амилоидное поражение печени может проявляться: - Увеличением печени. При пальпации живота определяется увеличенная, плотная, однако безболезненная печень. Поверхность ровная и гладкая.
- Портальной гипертензией. Кровь от большинства внутренних органов (от желудка, кишечника, селезенки и других) собирается в так называемую воротную (портальную) вену и поступает в печень (где происходит ее детоксикация). Только после этого она возвращается в системный кровоток. Сдавливание кровеносных сосудов печени отложениями амилоида приводит к повышению давления в системе воротной вены и расширению вен внутренних органов (с возможным их разрывом). Это может проявляться кровотечениями в желудочно-кишечном тракте, поносом и рвотой с кровью, отеками на ногах и асцитом.
- Желтухой. Крайне редкое проявление амилоидного поражения печени. Развивается при нарушении желчеобразующей функции органа либо в результате нарушения оттока желчи по желчевыводящим путям (сдавливаемым извне отложениями амилоида). В этом случае пигмент желтого цвета билирубин (являющийся продуктом распада клеток крови эритроцитов, который в норме удаляется из организма печенью) задерживается в крови, придавая кожным покровам и слизистым оболочкам желтоватый оттенок. Если желтуха обусловлена нарушением оттока желчи, она будет сопровождаться сильным кожным зудом.
Поражение сердца
Поражение сердечной мышцы чаще отмечается при первичном и некоторых формах наследственного амилоидоза. Отложение амилоида происходит не только в миокарде (
непосредственно сердечной мышце), но и в оболочках сердца – в перикардиальной сумке и эндокарде. Результатом этого является сдавливание кровеносных сосудов и нарушение кровообращения органа, что обуславливает гибель мышечных клеток.
Клинически амилоидоз сердца может проявляться: Аритмии Проводящая система сердца представляет собой особую группу мышечных клеток, которые обеспечивают последовательное проведение нервного импульса по сердечной мышце, в результате чего происходит синхронное сокращение предсердий и желудочков. В случае отложения амилоида в данной области проведение нервного импульса нарушается, в результате чего камеры сердца начинают сокращаться разобщено, то есть развивается аритмия. Клинически это может проявляться потемнением перед глазами, частыми головокружениями и
обмороками, что обусловлено нарушением кровоснабжения головного мозга и может привести к смерти больного.
Рестриктивная кардиомиопатия В результате отложения амилоида миокард уплотняется и становится менее растяжимым. Во время диастолы (
расслабления сердечной мышцы) камеры сердца не могут расшириться в достаточной степени и вместить необходимый объем крови, что приводит к уменьшению ударного объема (
количества крови, выбрасываемой сердцем во время сокращения).
Клинически данное состояние проявляется повышенной утомляемостью,
одышкой (
развивающейся из-за скопления крови в легочных сосудах) и отеками ног (
возникающими из-за скопления крови в венах нижних конечностей), асцитом и гидротораксом (
в результате повышения давления в сосудах кровь пропотевает в полости организма). Частым симптомом является ортостатическая гипотензия, то есть снижение артериального давления при резком переходе из горизонтального положения в вертикальное, что обусловлено снижением приспособительных реакций сердечной мышцы.
По мере прогрессирования заболевания наполнение сердца еще больше снижается, что в конечном итоге приводит к развитию сердечной недостаточности.
Сердечная недостаточность Характеризуется неспособностью сердца обеспечивать циркуляцию крови в организме, что клинически проявляется более выраженными отеками (
преимущественно в нижней части тела, усиливающимися к вечеру), одышкой и другими симптомами. Характерной особенностью сердечной недостаточности при амилоидозе является неэффективность стандартного лечения, быстрое прогрессирование заболевания и смерть пациента в течение нескольких месяцев.
Надпочечниковая недостаточность
Надпочечники представляют собой небольшие железы, располагающиеся у верхнего края каждой почки и выделяющие гормоны. В надпочечниках выделяют корковое и мозговое вещество, каждое из которых вырабатывает определенные гормоны.
При амилоидозе депозиты амилоида откладываются по ходу сосудов исключительно в корковом веществе, в результате чего развивается хроническая надпочечниковая недостаточность, характеризующаяся уменьшением или полным прекращением синтеза всех гормонов данной области.
Характеристика надпочечниковой недостаточности при амилоидозе
| Гормоны коркового вещества надпочечников | Функция в организме | Нарушения, возникающие при недостаточности данного гормона |
| Альдостерон | - Участвует в регуляции водно-солевого обмена.
- Уменьшает скорость выделения натрия и воды почками, что приводит к увеличению объема циркулирующей крови (ОЦК) и повышению артериального давления.
- Задерживает калий и водород в организме.
| - Уменьшение ОЦК – проявляется слабостью, повышенной утомляемостью, головными болями и учащенным сердцебиением.
- Повышение концентрации калия в организме – может проявляться сердечными аритмиями, судорогами, головокружениями (вплоть до потери сознания).
|
| Кортизол | Регулирует обмен веществ в организме во время стрессовых ситуаций, а именно: - повышает концентрацию глюкозы в крови;
- стимулирует распад жиров;
- угнетает мочеобразование;
- обладает противовоспалительным действием.
| При недостатке кортизола нарушаются адаптационные (приспособительные) функции организма, в результате чего человек чаще болеет и тяжелее переносит различные заболевания, инфекции, травмы и так далее. |
Андрогены
(мужские половые гормоны) | Влияют на развитие вторичных половых признаков (роста бороды и усов, низкого тембра голоса и других) у мальчиков в подростковом возрасте. | - У мужчин наблюдается оволосение по женскому типу.
- У женщин происходит выпадение волос в лобковой и подмышечных областях.
|
Увеличение селезенки
Отложение амилоида в селезенке приводит к увеличению органа в размерах, в результате чего он может быть пропальпирован (
в норме при пальпации селезенка не определяется). При пальпации амилоидная селезенка плотная, поверхность гладкая и ровная, болезненность не определяется.
Как говорилось ранее, селезенка участвует в удалении «старых» и деформированных клеток крови из кровотока. Это происходит благодаря наличию в структуре органа так называемых синусоидов, представляющих собой тонкие щелевидные пространства. Нормальные клетки крови пластичны и с легкостью проходят через них, в то время как старые и поврежденные застревают и разрушаются. Отложение амилоида в селезенке приводит к развитию гиперспленизма, то есть в увеличенной селезенке начинают задерживаться и разрушаться нормальные, неповрежденные клетки крови – эритроциты (
транспортирующие дыхательные газы),
тромбоциты (
отвечающие за остановку кровотечений) и лейкоциты.
Гиперспленизм характеризуется: - Анемией – проявляется общей слабостью, бледностью кожных покровов и слизистых оболочек, иногда одышкой (чувством нехватки воздуха).
- Тромбоцитопенией – уменьшением концентрации тромбоцитов, что может проявляться кожными кровоизлияниями, кровотечениями из носа, кровоточивостью десен и так далее.
- Лейкопенией – уменьшением общего количества лейкоцитов, что проявляется частыми инфекциями, тяжело поддающимися лечению.
Поражение желудочно-кишечного тракта
При генерализованных формах амилоидоза поражение кишечника носит распространенных характер, в результате чего нарушается всасывание многих питательных веществ,
витаминов и минералов.
Нарушение всасывания в кишечнике может проявляться: - частым поносом;
- снижением веса (вплоть до кахексии – крайней степени истощения, представляющей непосредственную опасность для жизни);
- общей и мышечной слабостью;
- повышенной утомляемостью;
- умственными и психическими расстройствами;
- анемией (в результате нарушения всасывания железа, витамина B12 и фолиевой кислоты);
- ломкостью и выпадением волос;
- отеками (из-за снижения количества белков в крови).
В случае локальных форм амилоидоза отложения амилоида могут скапливаться в одном месте, имитируя опухоль. Увеличиваясь в размерах, они сдавливают петли кишечника и нарушают проходимость пищи по ним, в результате чего на первый план будут выступать симптомы
кишечной непроходимости –
запоры,
вздутие и
боли в животе, рвота каловыми массами (
в тяжелых случаях).
Поражение нервной системы
Отложения амилоида по ходу нервных волокон приводит к нарушению их функции, что будет проявляться соответствующими симптомами (
в зависимости от того, какой нерв и в какой области был поражен). Старческий амилоидоз, например, характеризуется отложением амилоида в ткани головного мозга, что чаще проявляется нарушением умственных способностей (
снижением концентрации внимания, нарушением интеллекта, снижением памяти) и психическими отклонениями. В то же время поражение периферических нервов при различных формах семейного амилоидоза может проявляться чувством ползания мурашек, болезненностью, зудом и нарушением чувствительности в определенных участках тела, вплоть до развития паралича конечностей (
полной утраты двигательной функции).
Поражение кожи
При отложении амилоида в структурах и сосудах кожи нарушается ее кровоснабжение, что проявляется бледностью, сухостью и шелушением. При определенных формах заболевания (
при генерализованном и некоторых формах локального амилоидоза) может появляться
сыпь в виде множества мелких (
1 – 2 мм) и плотных узелков желтого или красного цвета, которые могут сливаться, в результате чего площадь поражения может достигать значительных размеров. Иногда над поверхностью узелков определяется шелушение, однако болезненность и зуд встречаются довольно редко.
Поражение суставов
В результате отложения амилоида в суставах происходит их воспаление, причем вначале поражаются более мелкие суставы (
кистей и стоп), а по мере прогрессирования заболевания вовлекаются и более крупные (
коленные, локтевые).
Поражение суставов при амилоидозе характеризуется: - Болезненностью, усиливающейся при движениях.
- Покраснением кожи над поверхностью пораженных суставов, появляющейся из-за расширения сосудов в очаге воспаления.
- Отеком тканей, который развивается в результате пропотевания жидкости через стенки расширенных сосудов.
- Повышением температуры кожи в области воспаленных суставов.
- Нарушением функции пораженного сустава.
Поражение мышц
Отложение депозитов амилоида происходит в межмышечной соединительной ткани, в результате чего функция мышц длительное время не страдает (
так как структура мышечных клеток не нарушается). При прогрессировании заболевания происходит сдавливание мышечных клеток, нарушение их кровоснабжения и гибель.
Амилоидное поражение мышц проявляется: - болями в мышцах;
- мышечной слабостью;
- гипертрофией мышц (увеличением в размерах);
- появлением плотных узелков на поверхности мышц;
- уплотнением мышц («каменистой» плотностью).
Диагностика амилоидоза
![]()
Амилоидоз можно заподозрить на основании клинических проявлений заболевания, однако для подтверждения диагноза и назначения лечения необходимо провести целый ряд дополнительных лабораторных и инструментальных исследований.
В диагностике амилоидоза применяется: Общий анализ крови
Простое и недорогое исследование, позволяющее выявить отклонения в составе периферической крови пациента и на их основании предположить причину развития амилоидоза. Кроме того, на поздних стадиях заболевания определенные изменения в общем анализе крови будут указывать на повреждение того или иного органа, что позволит назначить более адекватное лечение. Кровь для общего анализа можно брать как из пальца, так и из вены.
Общий анализ крови при амилоидозе
| Показатель | Что обозначает | Норма | Возможные изменения при амилоидозе |
Концентрация эритроцитов
(RBC) | Эритроциты – красные клетки крови, которые транспортируют дыхательные газы (кислород и углекислый газ) в организме. | Мужчины (М):
4,0 – 5,0 х 1012/л. | Уменьшение концентрации эритроцитов отмечается на поздних стадиях амилоидоза и обычно являться признаком: - нарушения всасывания при амилоидозе кишечника;
- кровотечения из желудочно-кишечного тракта;
- терминальной стадии почечной недостаточности;
- поражения красного костного мозга амилоидозом;
- гиперспленизма.
|
Женщины (Ж):
3,5 – 4,7 х 1012/л. |
Общий уровень гемоглобина
(HGB) | Гемоглобин – содержащий железо дыхательный пигмент, который непосредственно участвует в транспортировке дыхательных газов. | М: 130 – 170 г/л. | Снижение уровня гемоглобина происходит по тем же причинам, что и снижение концентрации эритроцитов. |
| Ж: 120 – 150 г/л. |
Концентрация лейкоцитов
(WBC) | Основной функцией лейкоцитов является защита организма от инфекций. | 4,0 – 9,0 х 109/л. | - Повышение концентрации лейкоцитов может отмечаться при вторичном амилоидозе.
- При гиперспленизме общее количество лейкоцитов будет снижено.
|
Концентрация тромбоцитов
(PLT) | Тромбоциты обеспечивают остановку кровотечений из мелких сосудов, а также предотвращают выход крови из сосудистого русла. | 180 – 320 х 109/л. | При развитии гиперспленизма концентрация тромбоцитов резко снижается. |
Концентрация ретикулоцитов
(RET) | Ретикулоциты представляют собой молодые формы эритроцитов, которые образуются в костном мозге, после чего выделяются в системный кровоток, где и превращаются в зрелые эритроциты. | М: 0,24 – 1,7%. | Причиной снижения концентрации ретикулоцитов может быть: - нарушение всасывания в кишечнике;
- терминальная стадия почечной недостаточности;
- поражение костного мозга амилоидозом.
Причиной компенсаторного повышения концентрации ретикулоцитов может быть: - кровотечение из желудочно-кишечного тракта;
- гиперспленизм.
|
| Ж: 0,12 – 2,05%. |
Гематокрит
(Hct) | Гематокрит – процентное соотношение между клеточными элементами крови и объемом плазмы. | М: 42 – 50%. | Так как основная масса клеточных элементов крови представлена эритроцитами, снижение их концентрации приведет к снижению гематокрита. |
| Ж: 38 – 47%. |
Скорость оседания эритроцитов
(СОЭ) | На поверхности клеток крови имеются определенные отрицательные заряды, вследствие чего они отталкиваются друг от друга и находятся во взвешенном состоянии. Если поместить кровь в пробирку, тот через некоторое время более тяжелые эритроциты осядут на ее дно. Время, за которое это произойдет и будет скоростью оседания эритроцитов. | М: 3 – 10 мм/час. | СОЭ может увеличиваться при развитии анемии, а также при наличии в крови белков острой фазы воспаления, что является признаком системного воспалительного процесса и может указывать на вторичную природу амилоидоза. |
| Ж: 5 – 15 мм/час. |
Общий анализ мочи
Изменения в общем анализе мочи могут наблюдаться при почечном амилоидозе, а также при хронических воспалительных
заболеваниях почек.
На поражение почек может указывать: - Протеинурия (появление белка в моче). Является первым и наиболее значимым проявлением поражения почек при амилоидозе. В норме концентрация белка в моче не превышает 0,033 г/л, однако при нарушении целостности почечного фильтра клетки крови и крупномолекулярные белки начинают выделяться с мочой. Протеинурия более 3 г/л свидетельствует о выраженном нефротическом синдроме и тяжелом поражении почечной ткани.
- Гематурия (появление эритроцитов в моче). В норме при микроскопическом исследовании мочи допускается не более 1 – 3 эритроцитов в поле зрения. Кровь в моче может указывать на развитие нефротического синдрома либо являться признаком воспалительного поражения почечной ткани (гломерулонефрита).
- Лейкоцитурия (появление лейкоцитов в моче). При микроскопическом исследовании мочи допускается наличие 3 – 5 лейкоцитов в поле зрения. Лейкоцитурия редко наблюдается при почечном амилоидозе и чаще свидетельствует о наличии инфекционно-воспалительного заболевания почек или других органов мочеполовой системы.
- Цилиндрурия (наличие цилиндров в моче). Цилиндры представляют собой слепки, которые образуются в почечных канальцах и имеют различную структуру. При амилоидозе они обычно образуются из слущенных клеток почечного эпителия и белков (гиалиновые цилиндры), однако могут также содержать эритроциты и лейкоциты.
- Снижение плотности мочи. Нормальная плотность мочи колеблется в пределах от 1,010 до 1,022, однако при разрушении почечных нефронов концентрационная способность органа заметно снижается, в результате чего плотность мочи будет уменьшаться.
Биохимический анализ крови
Данное исследование позволяет не только оценить функциональное состояние внутренних органов, но и заподозрить причину амилоидоза.
Диагностическую ценность при амилоидозе представляют: Белки общей фазы воспаления Данные белки вырабатываются печенью и некоторыми лейкоцитами в ответ на развитие воспалительного процесса в организме. Главной их функцией является поддержание воспаления, а также предупреждение повреждения здоровых тканей.
Белки острой фазы воспаления
| Белок | Нормальные значения |
| Сывороточный белок амилоида А (SAA) | Менее 0,4 мг/л. |
| Альфа-2-глобулин | М: 1,5 – 3,5 г/л. |
| Ж: 1,75 – 4,2 г/л. |
| Альфа-1-антитрипсин | 0,9 – 2 г/л. |
| С-реактивный белок | Не более 5 мг/л. |
| Фибриноген | 2 – 4 г/л. |
| Лактоферрин | 150 – 250 нг/мл. |
| Церулоплазмин | 0,15 – 0,6 г/л. |
Следует отметить, что прогрессирующее повышение концентрации фибриногена в крови часто встречается и при наследственных формах амилоидоза, что необходимо учитывать при оценке данного показателя.
Печеночные пробы В данную группу входит ряд показателей, позволяющих оценить функциональное состояние печени.
Печеночные пробы при амилоидозе печени
| Показатель | Что обозначает | Норма | Изменения при амилоидозе печени |
| Аланинаминотрансфераза (АлАТ) | Данные вещества содержатся в клетках печени и попадают в кровоток в большом количестве лишь при массивном разрушении ткани органа. | М: до 41 Ед/л. | Концентрация повышается при развитии печеночной недостаточности. |
Ж: до 31 Ед/л.
|
| Аспартатаминотрансфераза (АсАТ) |
| Билирубин общий | При распаде эритроцитов в селезенке происходит образование несвязанного билирубина. С током крови он поступает в печень, где связывается с глюкуроновой кислотой и в таком виде выделяется из организма в составе желчи. | 8,5 – 20,5 мкмоль/л. | Концентрация повышается при массивном отложении амилоида в печени. |
Билирубин
(несвязанная фракция) | 4,5 – 17,1 мкмоль/л. | Концентрация повышается при печеночной недостаточности и нарушении желчеобразующей функции органа. |
Билирубин
(связанная фракция) | 0,86 – 5,1 мкмоль/л. | Концентрация повышается при сдавливании внутрипеченочных или внепеченочных желчевыводящих протоков. |
Уровень холестерина в крови Холестерин представляет собой вещество жировой природы, которое образуется в печени и играет важную роль в поддержании целостности мембран всех клеток организма. Увеличение концентрации холестерина в крови более 5,2 ммоль/л может наблюдаться при
нефротическом синдроме, причем, чем выше данный показатель, тем тяжелее протекает заболевание.
Уровень белков в крови Норма общего белка в крови составляет 65 – 85 г/л. Снижение данного показателя может наблюдаться при развитии нефротического синдрома (
в результате потери белка с мочой), а также при тяжелой печеночной недостаточности, так как все белки организма синтезируются в печени.
Уровень креатинина и мочевины Мочевина (
норма – 2,5 – 8,3 ммоль/л) представляет собой побочный продукт белкового обмена, который выделяется через почки. Креатинин (
норма – 44 – 80 мкмоль/л у женщин и 74 – 110 мкмоль/л у мужчин) образуется в мышечной ткани, после чего поступает в кровь и также выделяется почками. Увеличение концентрации данных веществ в крови является очень чувствительным показателем степени нарушения почечной функции при амилоидозе.
Ультразвуковое исследование внутренних органов
Данное исследование позволяет оценить строение и структуру внутренних органов, что необходимо для оценки степени нарушения их функции и определения распространенности патологического процесса.
УЗИ при амилоидозе может выявить: - Уплотнение и увеличение (или уменьшение в азотемической стадии) почек.
- Наличие почечных кист (что могло стать причиной вторичного амилоидоза).
- Увеличение и уплотнение печени и селезенки, а также нарушение кровотока в данных органах.
- Гипертрофию различных отделов сердечной мышцы.
- Отложения амилоида в стенках крупных сосудов (например, аорты – самой крупной артерии организма).
- Скопление жидкости в полостях организма (асцит, гидроторакс, гидроперикард).
Генетическое исследование
Генетическое исследование назначается при подозрении на наследственный амилоидоз (
то есть если не удается подтвердить вторичную природу данного заболевания). Обычно для этого используется полимеразная цепная реакция, принцип которой заключается во взятии генетического материала у больного человека (
обычно это кровь, моча, слюна или любая другая биологическая жидкость) и исследовании генов на определенных хромосомах. Выявление генетических мутаций в определенной области будет являться стопроцентным подтверждением диагноза.
При выявлении одной из форм наследственного амилоидоза генетическое исследование рекомендуется выполнить всем членам семьи и ближайшим родственникам больного, чтобы исключить наличие у них данного заболевания.
Биопсия
Биопсия представляет собой прижизненное взятие небольшого кусочка ткани или органа и исследование его в лаборатории с помощью специальных методик. Данное исследование является «золотым стандартом» в диагностике амилоидоза и позволяет подтвердить диагноз более чем в 90% случаев.
При амилоидозе для исследования может быть взята мышечная ткань, ткань печени, селезенки, почки, слизистой оболочки кишечника или другого органа (
в зависимости от клинической картины заболевания). Забор материала проводится в стерильной операционной, обычно под местным обезболиванием. С помощью специальной иглы с острыми краями производится прокол кожи и забор небольшого количества ткани органа.
В лаборатории часть полученного материала обрабатывают раствором Люголя (
йода в водном растворе йодида калия), а затем 10% раствором серной кислоты. При наличии большого количества амилоида он окрасится в сине-фиолетовый или зеленоватый цвет, что будет видно невооруженным глазом.
Для микроскопического исследования материал окрашивают специальными красителями (
например, конго красным, после которого амилоид приобретает специфический красный цвет), и исследуют под микроскопом, причем фибриллы амилоида четко определяются как хаотично располагающиеся палочковидные образования.
Лечение амилоидоза
Выявить амилоидоз и начать лечение на ранних этапах его развития довольно сложно, так как клинически заболевание проявляется через десятки лет после его начала. В то же время при выраженной почечной недостаточности лечебные мероприятия малоэффективны и носят поддерживающий характер.
Нужна ли госпитализация для лечения амилоидоза?
При подозрении на амилоидоз рекомендуется госпитализация в отделение нефрологи или терапии с целью проведения тщательного обследования мочеполовой системы, так как поражение почек является наиболее частым и в то же время наиболее опасным осложнением амилоидоза. Также должны быть привлечены специалисты из других областей медицины (
гепатолог, кардиолог, невролог и так далее) для выявления и лечения повреждений других органов и систем.
Если в процессе диагностики не выявлено серьезных функциональных нарушений со стороны каких-либо органов, дальнейшее лечение может проводиться в амбулаторных условиях (
на дому) при условии, что пациент будет строго соблюдать все предписания врача и являться на контроль как минимум 1 раз в месяц.
Основными показаниями для госпитализации являются: - наличие системного воспалительного процесса (подтвержденное лабораторно или клинически);
- наличие гнойного инфекционного заболевания;
- нефротический синдром;
- почечная недостаточность;
- печеночная недостаточность;
- сердечная недостаточность;
- надпочечниковая недостаточность;
- выраженная анемия (концентрация гемоглобина менее 90 г/л);
- гиперспленизм;
- внутреннее кровотечение.
Если в процессе амбулаторного лечения состояние пациента ухудшается, он также должен быть госпитализирован для уточнения диагноза и коррекции лечения.
В лечении амилоидоза применяется: - медикаментозное лечение;
- диетотерапия;
- перитонеальный диализ;
- пересадка органов.
Медикаментозное лечение
Медикаментозное лечение направлено на замедление процесса образования амилоида (
если это возможно). Хорошая эффективность наблюдается в случае AL-амилоидоза, в то время как при других формах заболевания добиться положительного результата удается не всегда. Хуже всего медикаментозному лечению поддается вторичный амилоидоз.
Медикаментозное лечение амилоидоза
| Группа препаратов | Представители | Механизм лечебного действия | Способ применения и дозы |
| Стероидные противовоспалительные препараты | Преднизолон | Угнетают иммунные реакции, обладают выраженным противовоспалительным действием. Снижают скорость образования лимфоцитов, а также тормозят миграцию лейкоцитов в очаг воспаления, чем и обусловлен положительный эффект при амилоидозе. | Дозировка, длительность применения и путь введения подбирается индивидуально в каждом конкретном случае в зависимости от тяжести основного и сопутствующих заболеваний. |
| Дексаметазон |
| Противоопухолевые препараты | Мелфалан | Нарушает процесс образования ДНК (дезоксирибонуклеиновой кислоты), что угнетает синтез белка и размножение клеток. Так как амилоидобласты в определенной степени считаются мутантными (опухолевыми) клетками, их уничтожение может замедлить процесс образования амилоида (особенно при первичной форме заболевания). | Внутрь, один раз в сутки в дозе 0,12 – 0,15 мг/кг. Длительность лечения 2 – 3 недели, после чего необходимо сделать перерыв (не менее 1 месяца). При необходимости курс лечения можно повторить. |
| Аминохинолиновые препараты | Хлорохин
(хингамин) | Противомалярийный препарат, который также тормозит синтез ДНК в клетках человеческого организма, уменьшая скорость образования лейкоцитов и амилоидобластов. | Внутрь, по 500 – 750 мг ежедневно или через день. Длительность лечения определяется эффективностью и переносимостью препарата. |
| Противоподагрические препараты | Колхицин | Угнетает скорость образования лейкоцитов и процесс синтеза амилоидных фибрилл в амилоидобластах. Эффективен при семейной средиземноморской лихорадке и в меньшей степени при вторичном амилоидозе. | Внутрь по 1 мг 2 – 3 раза в стуки. Лечение длительное (более 5 лет). |
Диетотерапия
Специфической
диеты, которая смогла бы предотвратить развитие амилоидоза или замедлить процесс образования амилоида не существует. Основными осложнениями амилоидоза, требующим соблюдения строгой диеты, являются нефротический синдром и почечная недостаточность. При развитии данных синдромов рекомендуется
диета номер 7, целью которой является защита почек от действия токсических продуктов обмена веществ, нормализация водно-солевого баланса и артериального давления.
Принимать пищу рекомендуется малыми порциями по 5 – 6 раз в сутки. Основным условием является ограничение потребления поваренной соли (
не более 2 грамм в сутки) и жидкости (
не более 2 литров в сутки), что в определенной степени предотвращает образование отеков и нормализует артериальное давление. Сложность в данном случае заключается в необходимости восполнять потери белка при нефротическом синдроме и в то же время уменьшить их потребление с пищей, так как при почечной недостаточности нарушается процесс выделения побочных продуктов их обмена.
Диета при амилоидозе
| Что рекомендуется употреблять? | Что не рекомендуется употреблять? |
- овощные бульоны;
- нежирные сорта мяса (говядины, телятины) не более 50 – 100 грамм в сутки;
- бессолевой хлеб и выпечку;
- свежие фрукты (яблоки, сливы, груши и т.д.);
- свежие овощи (помидоры, огурцы, картофель и т.д.);
- рис (не более 300 – 400 грамм в сутки);
- 1 – 2 яичных белка в сутки (без соли);
- молоко и кисломолочные продукты;
- некрепкий чай;
- свежевыжатые соки.
| - мясные и рыбные продукты в больших количествах;
- сдобную выпечку;
- некоторые фрукты (абрикосы, виноград, черешню и смородину);
- сухофрукты;
- сырные изделия;
- яичный желток;
- кофе;
- минеральные и газированные напитки;
- алкоголь.
|
Перитонеальный диализ
Принцип данного метода схож с принципом гемодиализа (
который описан ранее), однако существуют определенные различия. При перитонеальном диализе полупроницаемой мембраной, через которую происходит удаление побочных продуктов обмена веществ, является брюшина – тонкая, хорошо кровоснабжаемая серозная оболочка, выстилающая внутреннюю поверхность и органы брюшной полости. Общая площадь брюшины близка к площади поверхности тела человека. Специальный раствор вводится в брюшную полость через катетер (
трубку в животе) и вступает в контакт с брюшиной, в результате чего из крови в него начинают просачиваться продукты обмена веществ, то есть происходит очищение организма. «Недостатком» данного метода является более медленное очищение крови, чем при гемодиализе.
Основными преимуществами данного метода перед гемодиализом являются: - Выведение В2-микроглобулина, который может стать причиной развития амилоидоза.
- Постоянное (непрерывное) очищение крови от побочных продуктов обмена веществ.
- Возможность использования в амбулаторных условиях (на дому).
Техника выполнения Установка катетера выполняется в операционной под местным или общим обезболиванием. Обычно он устанавливается в нижней части брюшной стенки, причем наружу выходит лишь небольшое его отрезок. Через катетер в брюшную полость вводится около 2 литров специального диализирующего раствора, после чего катетер плотно закрывается и жидкость остается в брюшной полости на срок от 4 до 10 часов. В это время пациент может заниматься практически любой повседневной деятельностью.
Через установленные промежуток времени (
обычно каждые 6 – 8 часов) необходимо слить «старый» раствор из брюшной полости и заменить на новый. Вся процедура занимает не более 30 – 40 минут и требует минимальных усилий.
Перитонеальный диализ противопоказан: Пересадка органов
Пересадка донорских органов является единственным средством спасения жизни пациентов с развившейся органной недостаточностью. Однако стоит помнить, что данный метод лечения является лишь симптоматическим и не устраняет причину развития амилоидоза, поэтому в отсутствии постоянного адекватного лечения возможен рецидив заболевания.
При амилоидозе возможно пересадить: - почку;
- ткань печени;
- сердце;
- кожу.
Донорские органы могут быть получены от живого донора (
кроме сердца), а также от трупа либо от человека, у которого диагностирована смерть мозга, однако функциональная активность внутренних органов поддерживается искусственно. Кроме того, сегодня существует искусственное сердце, представляющее собой полностью механизированный аппарат, который может перекачивать кровь в организме.
Если донорский орган приживется (
что бывает не всегда), пациенту требуется пожизненное применение иммуносупрессоров (
препаратов, угнетающих активность иммунной системы), чтобы предотвратить отторжение «чужеродной» ткани собственным организмом.
Осложнения амилоидоза
![]()
К последствиям амилоидоза обычно относят различные острые состояния, развивающиеся на фоне нарушенных функций одного или нескольких органов. Зачастую данные осложнения становятся причиной смерти пациента.
Наиболее опасными осложнениями амилоидоза являются: - Инфаркт миокарда. При повышении системного артериального давления (всегда наблюдающемся при нефротическом синдроме и почечной недостаточности) нагрузка на сердечную мышцу возрастает в несколько раз. Данное состояние отягощается отложением амилоида в ткани сердца, что еще больше ухудшает его кровоснабжение. В результате этого при резкой физической нагрузке либо эмоциональном стрессе может развиться несоответствие между потребностью сердечной мышцы в кислороде и уровнем его доставки, что может привести к гибели кардиомиоцитов (мышечных клеток сердца). Если человек не погибает сразу (что наблюдается довольно часто), в зоне инфаркта формируется рубец, что еще больше «ослабляет» сердце (так как рубцовая ткань не способна сокращаться) и может привести к хронической сердечной недостаточности.
- Инсульт. Инсультом называется острое нарушение кровоснабжения ткани головного мозга. При амилоидозе данное состояние обычно развивается в результате кровотечения через деформированную стенку кровеносного сосуда (геморрагический инсульт). В результате пропитывания нервных клеток кровью они погибают, что в зависимости от зоны инсульта может проявляться самыми разными симптомами – от нарушения чувствительности и двигательной активности до смерти больного.
- Тромбоз печеночных вен. Данное осложнение может развиваться в результате повышения концентрации фибриногена (белка свертывающей системы крови) в системе почечных вен, что приводит к образованию тромбов, которые закупоривают просветы сосудов. В результате этого развивается острая почечная недостаточность. Механизм развития данного осложнения обусловлен тем, что при нефротическом синдроме через почки выделяется большое количество альбуминов (основных белков плазмы крови), в то время как фибриноген остается в крови и его относительная концентрация повышается.
- Инфекционные заболевания. Истощение защитных систем, потеря большого количества белков с мочой и развитие полиорганной недостаточности делает организм больного практически беззащитным перед различными патогенными микроорганизмами. При амилоидозе часто регистрируется пневмония (воспаление легких), пиелонефрит и гломерулонефрит, инфекции кожи (рожистое воспаление) и мягких тканей, пищевые токсикоинфекции, вирусные инфекции (например, паротит) и так далее.
![]()
Возможна ли беременность при амилоидозе?
Беременность при амилоидозе возможна только в тех случаях, когда функциональной активности жизненно важных органов женщины достаточно, для того чтобы выносить и родить ребенка. В противном случае беременность может закончиться смертью как плода, так и матери.
Некоторые локальные формы амилоидоза не представляют никакой опасности для беременности. Если скопление амилоида происходит лишь в одном органе или ткани (
например, в мышце или в стенке кишечника) и не достигает больших размеров, беременность и
роды будут протекать без осложнений, и ребенок родится абсолютно здоровым. В то же время при генерализованных формах амилоидоза прогноз для матери и плода целиком и полностью определяется длительностью заболевания и сохранившимися функциональными резервами жизненно-важных органов.
Исход беременности и родов определяется: - функциями сердца;
- функциями почек;
- функциями печени;
- функциями надпочечников;
- скоростью образования амилоида.
Функции сердца Опасным осложнением амилоидоза является сердечная недостаточность (
СН), развивающаяся из-за отложения амилоида в ткани сердца. Это приводит к нарушению его сократительной активности, в результате чего при нагрузках появляются определенные симптомы – слабость, одышка (
чувство нехватки воздуха), учащенное сердцебиение, боли за грудиной. Так как вынашивание ребенка и роды сопровождаются значительной нагрузкой на сердце, поражение данного органа может стать причиной развития серьезных осложнений во время беременности.
В зависимости от тяжести выделяют 4 функциональных класса СН. Первый характеризуется появлением симптомов лишь при крайне тяжелых физических нагрузках, в то время как четвертый выставляется пациентам, которые не могут самостоятельно себя обслуживать. Женщины с I – II функциональным классом могут спокойно выносить ребенка, однако им рекомендуется искусственное родоразрешение (
с помощью кесарева сечения). При наличии III – IV функционального класса беременность и роды абсолютно противопоказаны, так как организм в данном случае не сможет справиться с возрастающей нагрузкой. Вероятность гибели плода и матери в данном случае крайне велика, поэтому рекомендуется искусственное прерывание беременности (
аборт по медицинским показаниям).
Функции почек Развивающемуся плоду требуется постоянная доставка различных питательных веществ, в том числе и белков. Однако при отложении амилоида в почках матери происходит разрушение почечной ткани, вследствие чего клетки крови и крупномолекулярные белки начинают выделяться с мочой, что в конечном итоге приводит в выраженной белковой недостаточности, отекам и асциту (
скоплению жидкости в брюшной полости). Плод также начинает испытывать недостаток в белках (
являющихся основным строительным материалом для растущего организма), в результате чего может наблюдаться задержка в развитии, а после рождения могут отмечаться пороки развития, отставание в росте, умственные и психические отклонения.
Крайней степенью поражения почек при амилоидозе является хроническая почечная недостаточность, при которой почки не в состоянии удалять побочные продукты обмена веществ из организма. В результате этого они скапливаются в крови матери, оказывая токсическое влияние на все органы и системы, что может отразиться и на состоянии плода (
от легкой задержки развития до внутриутробной гибели).
Функции печени При отложении амилоида в ткани печени происходит сдавливание кровеносных сосудов органа, в результате чего повышается давление в системе так называемой воротной вены, которая собирает кровь от всех непарных органов брюшной полости (
от желудка, кишечника, селезенки и других). Вены данных органов расширяются, а их стенки истончаются. При дальнейшем повышении давления жидкая часть плазмы начинает выходить из сосудистого русла и скапливаться в брюшной полости, то есть развивается асцит. Если ее скапливается достаточно много, она начинает оказывать давление на растущий плод. Результатом этого может стать задержка в развитии, различные врожденные аномалии, а при выраженном напряженном асците (
если количество жидкости превышает 5 – 6 литров) может произойти внутриутробная гибель плода.
Функции надпочечников В нормальных условиях надпочечники секретируют определенные гормоны, участвующие в регуляции обменных процессов в организме. При поражении амилоидозом количество функциональной ткани в данных органах уменьшается, в результате чего заметно снижается продукция гормонов.
Во время беременности важную роль играет гормон надпочечников кортизол, функция которого заключается в активации приспособительных механизмов в организме матери. При его недостатке данные механизмы выражены крайне слабо или вовсе отсутствуют, в результате чего любая физическая или эмоциональная травма может привести к гибели плода и матери.
Скорость образования амилоида Обычно данный процесс протекает довольно медленно, ввиду чего от начала заболевания до развития полиорганной недостаточности проходит не менее десятка лет. Однако в некоторых случаях (
обычно при вторичном амилоидозе, развивающемся на фоне хронических гнойно-воспалительных процессов в организме) амилоид образуется очень быстро. Результатом этого может стать амилоидная инфильтрация сосудов плаценты (
органа, обеспечивающего обмен веществ между матерью и плодом), что приведет к кислородному голоданию плода, задержке его развития или даже к внутриутробной гибели.
Встречается ли амилоидоз у детей?
Дети болеют амилоидозом несколько реже, что, очевидно, связано со временем, необходимым для развития патологического процесса (
обычно для этого требуется несколько лет). Тем не мене, при некоторых формах наследственного амилоидоза, а также при вторичном амилоидозе возможно поражение внутренних органов в раннем детском возрасте.
Причиной амилоидоза у детей может быть: - Семейная средиземноморская лихорадка. Генетически обусловленное заболевание, наследующееся по аутосомно-рецессивному типу, то есть ребенок родится больным только в том случае, если унаследует дефектные гены от обоих родителей. Если же от одного родителя ребенок получит дефектный ген, а от второго – нормальный, он будет являться бессимптомным носителем заболевания, а его дети могут унаследовать дефектные гены с определенной долей вероятности. Клинически данный недуг проявляется генерализованным амилоидозом, который развивается в первые 10 лет жизни. Преимущественно поражается почечная ткань. Помимо амилоидоза наблюдаются приступы лихорадки (повышение температуры тела, озноб, повышенная потливость) и психические расстройства.
- Английский амилоидоз. Характеризуется преимущественным поражением почек, а также приступами лихорадки и потерей слуха.
- Португальский амилоидоз. В клинической картине преобладает поражение нервов нижних конечностей, что проявляется чувством ползания мурашек, нарушением чувствительности и двигательными расстройствами. Прогноз для жизни благоприятный, однако часто развивается паралич (неспособность выполнять произвольные движения).
- Американский амилоидоз. Характеризуется преимущественным поражением нервов верхних конечностей. Клинические проявления такие же, как при португальском амилоидозе.
- Вторичный амилоидоз. Данная форма заболевания развивается при наличии в организме хронических гнойно-воспалительных процессов (туберкулеза, остеомиелита, сифилиса и других). Если ребенок был заражен во время родов или сразу после рождения, вполне вероятно, что через 5 – 10 (а иногда и меньше) лет у него начнут появляться первые признаки генерализованного амилоидоза. Прогноз в данном случае крайне неблагоприятен – довольно быстро развивается полиорганная недостаточность и наступает смерть. Проводимое лечение дает положительные результаты лишь в половине случаев и на короткий промежуток времени, после чего заболевание обычно рецидивирует (обостряется повторно).
Существует ли эффективная профилактика амилоидоза?
Эффективность первичной профилактики (
направленной на предотвращение развития заболевания) зависит от формы амилоидоза и своевременности профилактических мероприятий. Вторичная профилактика (
направленная на предупреждение рецидивов заболевания) малоэффективна и не дает желаемых результатов.
Профилактика амилоидоза
| Форма амилоидоза | Краткая характеристика | Профилактические мероприятия |
| Первичный (идиопатический амилоидоз) | Причина данной формы заболевания неизвестна. | Отсутствуют. |
| Наследственный амилоидоз | Развитие амилоидоза в данном случае связано с наличием мутантных генов на определенных хромосомах (в генетическом аппарате человека их всего 23 пары). Данные гены передаются из поколения в поколение, в результате чего все потомство больного человека с определенной долей вероятности может заболеть амилоидозом. Дефектные гены запускают образование мутантных клеток (амилоидобластов), синтезирующих фибриллярные белки, которые впоследствии превращаются в амилоид и откладываются в тканях организма. | - Так как заболевание возникает еще при зачатии ребенка (при слиянии 23 материнских и 23 отцовских хромосом), постнатальная профилактика (проводимая после рождения ребенка) неэффективна.
- Единственным эффективным мероприятием является генетическое исследование плода на ранних сроках внутриутробного развития (до 22 недели беременности). При выявлении генов, отвечающих за развитие амилоидоза, рекомендуется прерывание беременности по медицинским показаниям.
- Если кто-либо из ближайших родственников человека болел амилоидозом, ему с супругой (супругом) также рекомендуется пройти генетическое обследование с целью выявления скрытой формы заболевания (носительства).
|
| Вторичный амилоидоз | Развитие данной формы заболевания возникает при хроническом воспалительном процессе в организме – при гломерулонефрите (воспалении почечной ткани), туберкулезе, остеомиелите (гнойном процессе в костной ткани) и других. В данном случае в крови повышается концентрация особого белка – сывороточного предшественника амилоида, который и обуславливает развитие заболевания. | Профилактика заключается в своевременном и полноценном лечении хронических воспалительных и гнойных процессов в организме. Это осуществляется с помощью применения антибактериальных препаратов широкого спектра действия (пенициллинов, цефтриаксона, стрептомицина, изониазида и других) до исчезновения клинических и лабораторных проявлений заболевания, а также в течение определенного периода времени после полного излечения. |
Сколько живут люди с амилоидозом?
При наличии развернутой клинической картины амилоидоза (
с явлениями полиорганной недостаточности) прогноз, в общем, неблагоприятный - более половины пациентов умирает в течение первого года после постановки диагноза. Однако чаще удается диагностировать заболевание в более ранние сроки. В таком случае прогноз для жизни определяется формой амилоидоза, а также выраженностью поражения жизненно-важных органов. При любой форме заболевание протекает более тяжело у людей в старческом возрасте.
На выживаемость пациентов с амилоидозом влияет: - Функция почек. При развитии почечной недостаточности пациент погибает в течение нескольких месяцев. Гемодиализ (очищение крови с помощью специального аппарата) продлевает жизнь больного на 5 лет и более. Пересадка почки может стать эффективным методом лечения, однако отложение амилоида в донорском органе наблюдаются более чем в половине случаев.
- Функция печени. При выраженной портальной гипертензии (повышении давления в системе воротной вены) происходит расширение вен внутренних органов (кишечника, пищевода, желудка). Пациент с такой симптоматикой может умереть в любой момент в результате кровотечения из разорвавшейся вены. Длительность жизни таких больных без радикального лечения (пересадки печени) не превышает 1 – 2 лет.
- Функция сердца. При развитии сердечной недостаточности VI степени большинство пациентов умирает в течение 6 месяцев. Пересадка сердца может продлить жизнь больных (при условии, что остальные органы и системы функционируют нормально).
- Функцией кишечника. При амилоидозе кишечника нарушение всасывания может достигать крайней степени выраженности. В отсутствии специфического лечения (полноценного внутривенного питания) смерть пациента может наступить уже через несколько недель из-за крайней степени истощения организма (кахексии).
В зависимости от формы заболевания выделяют: - Идиопатический генерализованный амилоидоз. Причина заболевания неизвестна. Проявляется поражением всех органов и тканей, быстрым развитием полиорганной недостаточности и смертью больного. Через год после постановки диагноза в живых остается лишь 51 человек из ста. Пятилетняя выживаемость составляет 16%, в то время как десятилетняя – не более 5%.
- Наследственный амилоидоз. Если заболевание развивается в раннем детском возрасте – прогноз неблагоприятен. Смерть обычно наступает из-за почечной недостаточности в течение нескольких лет после установления диагноза.
- Вторичный амилоидоз. Прогноз определяется функциональным состоянием внутренних органов. Основной причиной смерти при данной форме заболевания также является хроническая почечная недостаточность.
Локальные (
местные) формы амилоидоза обычно представляют собой опухолевидные образования различных размеров (
от 1 – 2 до десятков сантиметров в диаметре). В процессе роста они могут сдавливать соседние органы, однако своевременное хирургическое лечение позволяет устранить заболевание. Угроза для жизни практически отсутствует.
Можно ли вылечить амилоидоз народными средствами?
Существуют народные методы, которые на протяжении многих лет применялись в лечении данного недуга. Однако стоит отметить, что самолечение при таком серьезном заболевании как амилоидоз может привести к самым нежелательным последствиям, поэтому перед началом применения народных рецептов настоятельно рекомендуется проконсультироваться с врачом.
При амилоидозе можно применять: - Травяной противовоспалительный настой. В состав входят свежие цветки полевой ромашки (обладают противовоспалительным и противомикробным действием), цветки бессмертника (обладают противовоспалительным действием, а также улучшают выделение билирубина с желчью), трава зверобоя (повышает физическую и психическую выносливость) и березовые почки (обладают мочегонным действием). Для приготовления настоя необходимо по 200 грамм каждого ингредиента поместить в стеклянную банку и залить литром кипятка. После этого плотно закрыть крышкой и оставить в темном месте на 5 – 6 часов. Принимать по 200 мл 1 раз в сутки перед сном. Длительность непрерывного лечения не более 3 месяцев.
- Настой из плодов рябины и черники. Для приготовления настоя необходимо взять по 100 грамм плодов каждой ягоды и залить литром кипятка. Через полчаса процедить, дать остынуть и принимать по 100 мл 3 раза в день перед едой. Настой обладает противовоспалительным и вяжущим действием.
- Настой из глухой крапивы. Данное растение содержит дубильные вещества, аскорбиновую кислоту, гистамин и много других веществ. Применяется при хронических инфекционных заболеваниях почек. Для приготовления настоя 3 – 4 ложки измельченной травы крапивы следует залить в термосе 500 миллилитрами горячей воды (не кипятком) и принимать по 100 миллилитров 4 – 5 раз в день.
- Настой из плодов можжевельника. Обладает противовоспалительным, противомикробным, желчегонным и мочегонным действием. Для приготовления настоя 1 столовую ложку сушеных ягод необходимо залить 1 литром кипятка и настаивать в темном месте в течение 2 – 4 часов. Принимать по 1 столовой ложке 3 – 4 раза в день перед едой.
- Настойка травы посевного овса. Обладает противовоспалительным и общетонизирующим действием. Повышает работоспособность и стрессоустойчивость организма. Для приготовления настойки необходимо 200 мг измельченной травы овса залить 70% спиртом и настаивать в темном месте в течение 3 недель, ежедневно взбалтывая банку. После этого процедить и принимать по 1 чайной ложке 3 раза в день, разбавляя в 100 мл теплой кипяченой воды.


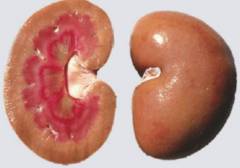 Амилоидоз – системное заболевание, характеризующееся нарушением белкового обмена и функционирования иммунной системы. В результате данных нарушений образуется специфический белково-сахаридный комплекс амилоид, который откладывается практически во всех тканях организма. По мере прогрессирования заболевания амилоид вытесняет нормальные клетки из пораженного органа, обуславливая развитие необратимых изменений и утрату функциональной активности. При длительном течении заболевания и в отсутствии лечения развивается полиорганная недостаточность (нарушение функции множества органов) и наступает смерть.
Амилоидоз – системное заболевание, характеризующееся нарушением белкового обмена и функционирования иммунной системы. В результате данных нарушений образуется специфический белково-сахаридный комплекс амилоид, который откладывается практически во всех тканях организма. По мере прогрессирования заболевания амилоид вытесняет нормальные клетки из пораженного органа, обуславливая развитие необратимых изменений и утрату функциональной активности. При длительном течении заболевания и в отсутствии лечения развивается полиорганная недостаточность (нарушение функции множества органов) и наступает смерть. Амилоидоз относится к диспротеинозам, то есть к болезням, протекающим с нарушением белкового обмена. В то же время доказано, что данное заболевание развивается лишь при нарушении функционирования иммунной системы, поэтому для понимания сути патологических процессов, происходящих в организме больного, необходимы определенные знания из области иммунологии и физиологии.
Амилоидоз относится к диспротеинозам, то есть к болезням, протекающим с нарушением белкового обмена. В то же время доказано, что данное заболевание развивается лишь при нарушении функционирования иммунной системы, поэтому для понимания сути патологических процессов, происходящих в организме больного, необходимы определенные знания из области иммунологии и физиологии. Амилоидоз может являться самостоятельным заболеванием либо развиться в результате патологии других органов и систем.
Амилоидоз может являться самостоятельным заболеванием либо развиться в результате патологии других органов и систем.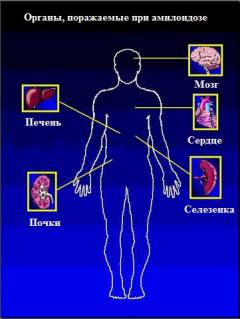 Исходя из того, что амилоидоз может поражать практически любой орган и ткань, симптомы данного заболевания могут быть самыми разнообразными. При различных формах амилоидоза вначале отмечается преимущественное поражение одного органа, что характеризуется нарушением его функции и развитием симптомов органной недостаточности. При прогрессировании заболевания процесс распространяется по всему организму, вовлекая другие ткани. Исключение составляет локальный амилоидоз, при котором поражается лишь один орган.
Исходя из того, что амилоидоз может поражать практически любой орган и ткань, симптомы данного заболевания могут быть самыми разнообразными. При различных формах амилоидоза вначале отмечается преимущественное поражение одного органа, что характеризуется нарушением его функции и развитием симптомов органной недостаточности. При прогрессировании заболевания процесс распространяется по всему организму, вовлекая другие ткани. Исключение составляет локальный амилоидоз, при котором поражается лишь один орган.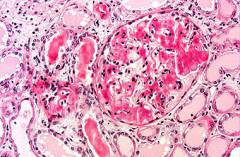 Амилоидоз можно заподозрить на основании клинических проявлений заболевания, однако для подтверждения диагноза и назначения лечения необходимо провести целый ряд дополнительных лабораторных и инструментальных исследований.
Амилоидоз можно заподозрить на основании клинических проявлений заболевания, однако для подтверждения диагноза и назначения лечения необходимо провести целый ряд дополнительных лабораторных и инструментальных исследований. К последствиям амилоидоза обычно относят различные острые состояния, развивающиеся на фоне нарушенных функций одного или нескольких органов. Зачастую данные осложнения становятся причиной смерти пациента.
К последствиям амилоидоза обычно относят различные острые состояния, развивающиеся на фоне нарушенных функций одного или нескольких органов. Зачастую данные осложнения становятся причиной смерти пациента.