![]() Апластическая анемия
Апластическая анемия является тяжелым
заболеванием крови, при котором развивается угнетение всех ростков костного мозга. Причины заболевания различные – от генетической предрасположенности до вредоносного действия ионизирующего излучения и различных химических соединений. Клинически заболевание проявляется анемическим, тромбоцитопеническим синдромом, а также выраженными инфекционными осложнениями.
Диагноз выставляется исходя из клинической картины, анализов крови и пункции костного мозга. Лечение в большинстве случаев предполагает пересадку здоровых стволовых клеток. Эффективность лечения зависит от множества факторов, основными из которых являются антигенная совместимость стволовых клеток донора и реципиента, внутренние резервы организма реципиента, качество посттрансплантационного ведения больного и др. Прогноз заболевания скорее отрицательный ввиду сложности нахождения подходящего донора костного мозга, высокого числа осложнений со стороны иммунной системы больного, высокой частоты развития инфекционных осложнений и острой полиорганной недостаточности.
Интересные факты - В теле взрослого человека содержится в среднем 25 – 30 х 1012 эритроцитов, что приблизительно равно 2 кг.
- Костный мозг производит в среднем 10 миллиардов эритроцитов в час.
- Благодаря особой форме и структуре эритроцит проходит через сосуды шириной 0,5 – 0,7 мкм.
- Впервые идея о пересадке костного мозга возникла в конце 19 века и успешно осуществилась в 1968 г. в США.
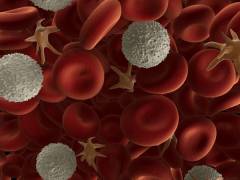
Что такое эритроциты, лейкоциты и тромбоциты?
![]()
Несмотря на то, что под анемией принято подразумевать снижение концентрации эритроцитов и\или
гемоглобина в периферической крови, в случае апластической анемии помимо описания эритроцитов необходимо кратко охарактеризовать
лейкоциты и
тромбоциты, поскольку при данном типе анемии происходит угнетение всех трех кроветворных ростков.
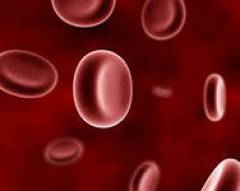
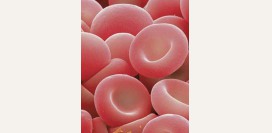
Эритроциты
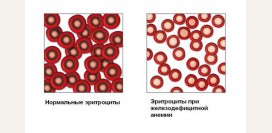
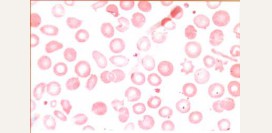
Эритроциты, или красные кровяные тельца, являются наиболее многочисленными клетками крови. Они представляют собой безъядерные клетки в форме двояковогнутого диска. При рассмотрении под микроскопом они выглядят как круги с просветлением посередине. Существуют определенные показатели нормального состояния эритроцита. В первую очередь, форма эритроцита, упомянутая выше. Измененная форма эритроцита часто указывает на определенные виды наследственных анемий. Наличие в крови измененных красных кровяных клеток различной формы называется пойкилоцитозом.
Диаметр эритроцита находится в пределах 7,2 – 7,5 мкм. Увеличение или уменьшение диаметра может свидетельствовать в пользу определенных видов анемий. Присутствие в периферической крови эритроцитов с различным диаметром именуется анизоцитозом.
Средний объем эритроцита равняется 90 мкм
3. Длительность жизни эритроцита составляет 90 – 120 дней. Физиологическая норма количества эритроцитов и концентрации гемоглобина зависит от пола. У мужчин – 3,9 – 5,2 х 10
12\л; у женщин – 3,7 – 4,9 х 10
12\л. Уровень гемоглобина у мужчин колеблется в пределах 130 – 160 г\л, у женщин – 120 – 150 г\л.
Особенности структуры эритроцита Внутри эритроцита, а точнее, в ячейках цитоскелета (
комплекс белков, обеспечивающих поддержание формы клетки) содержится вещество под названием гемоглобин. Подсчитано, что в одном эритроците может находиться от 280 до 400 миллионов молекул данного вещества. Гемоглобин представляет собой белковый комплекс, состоящий из белка глобина и гемма (
сложная молекула, в центре которой располагается железо). Основной функцией гемоглобина является перенос молекул кислорода к тканям и удаление из них углекислого газа. Существует несколько разновидностей гемоглобина (
Hb). Гемоглобин А (
HbA) является наиболее численной фракцией (
95 – 98%) и представляет собой обычный гемоглобин, находящийся в кровеносной системе взрослого человека. Гемоглобин А2 (
HbA2) является структурной модификацией стандартного гемоглобина и отличается некоторыми особенностями, проявляющимися в неблагоприятных условиях среды. Его количество равно 2 – 3% от общего пула эритроцитов. Гемоглобин F (
HbF) – фетальная фракция, у взрослых практически отсутствует (
1 – 2%), однако превалирует у новорожденных детей (
70 – 90%). К концу первого года жизни эритроциты, содержащие фетальный гемоглобин, разрушаются, а их место занимают эритроциты, заполненные взрослым HbA.
Мембрана эритроцита состоит из двойного слоя
липидов, пронизанных белками, выполняющими функцию транспорта ионов и поддержания оптимального электролитного равновесия. На поверхности клеточной мембраны располагается особый слой гликопротеидов, называющийся гликокаликс. Различные молекулы, входящие в его состав, играют роль рецепторов и антигенов гистосовместимости, отличающих эритроцит от других клеток организма. По приблизительным подсчетам на поверхности красных кровяных телец находится как минимум 250 видов различных антигенов, наиболее изученными из которых являются антигены системы АВ0 и
резус-фактора. Согласно системе АВ0 эритроциты разделяются на 4 группы, а по резус-фактору различают две группы. Данные группы исключительно важны при переливании крови или эритроцитарной массы от доноров к реципиентам.
По системе АВ0 различают 4 группы крови: - отсутствие агглютиногенов на поверхности эритроцитов;
- присутствие агглютиногенов А;
- присутствие агглютиногенов В;
- присутствие агглютиногенов А и В.
По резус-фактору различают 2 группы крови: - резус-положительная (у 85% населения);
- резус-отрицательная (у 15 % населения).
Однако даже при переливании крови пациентам с одинаковой группой крови по обеим группам антигенов случаются анафилактические реакции. Данный феномен объясняется несовместимостью крови донора и реципиента по остальным типам антигенов. Учитывая различные комбинации между ними, вероятность переливания абсолютно идентичной группы крови ничтожно мала. Практически со стопроцентной вероятностью можно утверждать, что, сколько на планете людей, столько и групп крови.
Гликокаликс на поверхности мембраны здорового эритроцита имеет еще одну важную особенность – отрицательный заряд. Благодаря тому, что поверхность всех эритроцитов носит одинаковый заряд, согласно законам физики происходит их взаимное отталкивание. Более того, эндотелиоциты (
клетки, выстилающие внутреннюю поверхность кровеносных сосудов) также обладают отрицательным зарядом. Таким образом, предотвращается слипание эритроцитов между собой и их прикрепление к стенкам сосудов, что, в свою очередь, снижает вероятность образования
тромбов. Соответственно, при нарушении метаболизма эритроцитов или при повреждении эндотелия сосудов возрастает риск образования тромбов.
Отличительной особенностью эритроцитов является их поразительная способность проникать через сосуды, диаметр которых менее диаметра эритроцита в 2 – 3 раза. С этой целью в процессе созревания эритроцита происходит разрушение его ядра и большинства органелл. Свойство эритроцита изменять свою форму называется деформируемостью и обеспечивается устойчивой работой цитоскелета клетки. Цитоскелет является системой продольных внутриклеточных белков, которые, выстраиваясь определенным образом, придают клетке необходимую форму и способствуют ее активному передвижению. Основными структурами цитоскелета являются микротрубочки и микрофиламенты, а белки, из которых они состоят, называются актин, миозин и тубулин. При необходимости удлинения и сужения эритроцита для прохождения через узкий сосуд происходит активное нагнетание в него ионов кальция, под действием которых происходит перестроение цитоскелета. После прохождения узкой зоны происходит выход кальция из клетки, приводящий к восстановлению его формы.
Однако в определенных случаях пластичность цитоскелета эритроцитов может ухудшаться, приводя к замедленному их прохождению по микроциркуляторному руслу и даже застреванию. При прохождении через
селезенку эритроциты с пониженной деформируемостью задерживаются в ее сосудах и уничтожаются клетками макрофагальной системы. Наиболее частыми причинами, ведущими к этому, являются высокие показатели гемоглобина при
эритремии, повышенная жирность крови и выход ее температуры за пределы оптимальных величин.
Как и любая живая клетка, эритроцит нуждается в питательных веществах для поддержания работоспособности. Занимательно то, что клетки, переносящие кислород во все уголки тела человека, не нуждаются в нем и соответственно не потребляют его в процессе транспортировки. Образование молекул АТФ (
аденозинтрифосфат), являющихся топливом для большинства ферментных систем клетки, происходит анаэробным, то есть безвоздушным путем. Таким образом, эритроциты абсолютно не чувствительны к недостатку кислорода, однако могут страдать от снижения уровня глюкозы в крови.
Помимо функции газообмена эритроциты выполняют еще ряд важных функций: - поддержание кислотно-щелочного равновесия крови – посредством карбонатной буферной системы, второй по важности в организме.
- определение реологии крови – посредством изменения численности клеточных элементов крови по отношению к жидкой части.
- гемостаз – участие в образовании тромба в месте повреждения сосудистой стенки.
- участие в иммунных процессах – посредством специфических рецепторов к иммуноглобулинам и комплементу на мембране эритроцита.
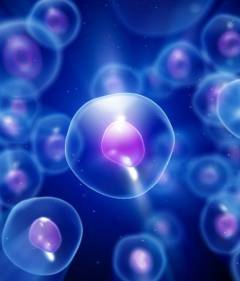
Созревание и старение эритроцита Первичной клеткой, из которой происходит рост и дифференцировка эритроцита, является стволовая мультипотентная клетка. Из всех клеток организма она обладает наиболее высоким потенциалом к делению и самым широким спектром возможностей к дифференцировке. Иными словами, она является клеткой предшественницей всех тканей организма, и поэтому уровень ее дифференцированности приравнивается к нулевому. При стимуляции малоизученными наукой медиаторами данная клетка трансформируется в тотипотентные клетки, способность которых к размножению также велика, а уровень дифференцированности выше. Впоследствии при дальнейшей дифференцировке тотипотентной клетки образуется колониеобразующая единица эритроцитарного ряда, иначе именуемая эритроцитарным ростком, являющимся непосредственным и первым предшественником красных кровяных телец.
По мере созревания клетки состав ее органелл значительно изменяется, среда из кислой становится нейтральной, а затем щелочной. Эти изменения соответствуют стадиям проэритробласта и эритробласта. Непосредственным предшественником эритроцита является ретикулоцит. Данная клетка в начале своего развития располагается в костном мозге в течение 24 – 30 часов, после чего выходит в кровеносное русло и дозревает в течение 36 – 44 часов. Отличительной особенностью данных клеток является больший размер по сравнению с эритроцитом, скопления распавшегося ядра в виде небольших включений, незначительная сине-фиолетовая исчерченность. По мере полного созревания ретикулоцита его размер уменьшается за счет удаления из клетки остатков ядра и органелл, связанных с синтезом веществ. Освободившееся место занимается молекулами гемоглобина, располагающимися в ячейках цитоскелета. В сформировавшемся эритроците еще в течение некоторого времени происходит синтез гемоглобина из остаточных цепей матричной РНК. По мере ее распада все синтетические процессы замирают, и эритроцит переходит в режим полноценной работы и параллельного поддержания жизнеспособности.
Регуляция роста и дифференцировки всех клеток эритроидного ряда осуществляется при непосредственном влиянии эритропоэтина. Данное вещество является одним из гормонов, синтезируемых почками. Точкой приложения его действия является проэритробласт. Регуляция осуществляется по механизму обратной связи. Иными словами, при снижении количества эритроцитов или гемоглобина в периферической крови происходит компенсаторный выброс эритропоэтина и наоборот – при высокой концентрации гемоглобина и эритроцитов образование эритропоэтина приостанавливается. Эритропоэтин стимулирует рост, размножение и дифференцировку клеток эритроидного ряда, непосредственно воздействуя на них. Косвенная регуляция скорости эритропоэза (
процесс образования эритроцитов в костном мозге) осуществляется посредством фактора стволовых клеток, интерлейкиа-3, витамина В12, микроэлементов (
цинк, медь, железо, селен и др.), гормонов (
соматостатин, тироксин, кортикостероиды и половые гормоны).
По прошествии 90 – 120 дней ферментные системы эритроцита постепенно изнашиваются, в результате чего размеры эритроцита уменьшаются, а содержание гемоглобина остается без существенных изменений. В результате происходит относительное повышение вязкости цитоплазмы, при котором относительная концентрация гемоглобина составляет 360 – 380 г\л. Возрастает и плотность эритроцита, которая отражается в снижении его деформируемости. При прохождении через узкие сосуды селезенки старые непластичные эритроциты застревают в них, поглощаются и разрушаются макрофагами.
Лейкоциты
Лейкоциты, или белые кровяные тельца, изначально были выделены в отдельную подгруппу, поскольку содержали ядро и не имели собственной окраски. Данный тип клеток подразделяется на множество видов по форме и выполняемой функции. Их деятельность можно резюмировать в обеспечении активных и пассивных иммунных реакций организма. На поверхности лейкоцитов находятся два комплекса гистосовместимости. Первый хранит информацию о собственных тканях организма, препятствуя их разрушению. Второй содержит информацию об антигенах чужеродных веществ, которые когда-либо попадали в организм, для того чтобы при встрече незамедлительно их атаковать.
Лейкоциты обладают способностью к самостоятельному передвижению в направлении увеличения концентрации определенного вещества. Такое движение называется хемотаксисом. Веществами, притягивающими лейкоциты, являются биологически активные соединения, высвобождающиеся при разрушении любых других лейкоцитов в процессе борьбы с патогенными
бактериями, простейшими, грибками и
вирусами, попавшими в организм. Физиологическая норма лейкоцитов 4 – 9 х 10
9\л.
Длительность жизни лейкоцитов разнообразна и зависит преимущественно от функции, которую выполняет клетка. В среднем она колеблется от нескольких десятков дней до нескольких десятков лет. Образование лейкоцитов происходит в красном костном мозге из общего лейкоцитарного ростка. Первичное обучение, в процессе которого лейкоциты приобретают первый комплекс гистосовместимости, осуществляется в тимусе. Вторичное обучение, в процессе которого лейкоциты приобретают второй комплекс гистосовместимости, осуществляется в периферических лимфатических узлах.
Тромбоциты
Тромбоциты являются третьей и последней разновидностью клеточных элементов крови. Сразу же необходимо заметить, что тромбоциты не являются самостоятельными клетками. Их образование происходит также в красном костном мозге из клеток, называемых мегакариоцитами. Мегакариоцит представляет собой наиболее крупный кроветворный росток по сравнению с эритроцитарным и лейкоцитарным. В диаметре он может достигать 20 – 25 мкм. В центре мегакариоцита располагается крупное ядро. В цитоплазме синтезируется большой спектр биологически активных веществ, которые впоследствии становятся содержимым тромбоцита. Клеточная мембрана образует множество выростов, края которых постоянно отрываются. Мембраны оторвавшихся фрагментов смыкаются, образуя то, что, по сути, и является тромбоцитом.
Тромбоцит выполняет преимущественно функцию гемостаза – сохранения целостности кровеносного русла. Он первый среди остальных клеточных элементов реагирует на повреждение сосудистой стенки и образует первичный тромб, к усилению которого впоследствии привлекаются лейкоциты и эритроциты. Располагаясь непосредственно над сосудистым дефектом, тромбоциты формируют мелкую сеть, в которую попадают эритроциты и лейкоциты. Таким образом образуется сгусток. По мере закрытия сгустком всей поврежденной поверхности тромбоциты выделяют определенные вещества, приводящие к стягиванию сети и ретракции сгустка. При этом из него удаляется большая часть жидкости, а сам тромб становится плотнее.
По данным последних исследований обнаружена еще одна важнейшая функция тромбоцитов, которая заключается в стимуляции процессов роста и регенерации тканей в поврежденной области. Таким образом, тромбоцит играет роль не только в обеспечении гемостаза, но еще и в росте и функциональном восстановлении поврежденных тканей. Физиологическая норма тромбоцитов находится в пределах 180 – 320 х 10
9\л.
Что такое апластическая анемия?
![]()
Апластическая анемия является патологическим состоянием организма, при котором снижается количество всех трех типов клеток крови (
эритроцитов, лейкоцитов и тромбоцитов) вследствие замедления или полного прекращения образования их в костном мозге.
По происхождению апластические анемии делятся на: - врожденные;
- приобретенные.
В большинстве случаев наблюдается угнетение всех трех ростков кроветворения, однако клинически замечено, что в различные фазы болезни может наблюдаться более выраженное угнетение какого-то одного из ростков. В подтверждение этому был проведен ряд экспериментов, в результате которых было продемонстрировано различное по выраженности эффекта влияние разнообразных неблагоприятных факторов на костный мозг.
По преимущественному поражению костномозговых ростков выделяют: - угнетение одного кроветворного ростка (эритроцитарного, лейкоцитарного или тромбоцитарного);
- угнетение двух кроветворных ростков;
- угнетение трех кроветворных ростков.
Подпишитесь на Здоровьесберегающий видеоканал


Причины апластической анемии
![]()
Причины апластической анемии различаются при врожденной и приобретенной анемии. Соответственно причине, некоторые анемии являются частично обратимыми. Иными словами, при снижении интенсивности факторов, повреждающих костный мозг, может произойти частичное восстановление кроветворения.
Наиболее распространенным видом врожденной апластической анемией является анемия Фанкони. Непосредственной причиной заболевания является повышенная чувствительность
ДНК клеток к повреждающим агентам. Данное заболевание наследуется по аутосомно-рецессивному типу. Это значит, что, для того чтобы оно проявилось, необходимо, чтобы у обоих родителей присутствовал дефект причинного гена. Лишь только в подобном случае вероятность развития клинических признаков заболевания у ребенка составляет приблизительно 25%. Соответственно, предотвратить данное заболевание можно, если заранее знать, что в роду обоих родителей имелись больные данным типом анемии, и предостеречь данную пару от
зачатия ребенка.
Различают следующие причины приобретенных апластических анемий: - ионизирующее излучение;
- лекарственные препараты (декарис, анальгин, левомицетин, тетрациклин, бутадион и др.);
- химические соединения (пестициды, бензол);
- заболевания (вирусные гепатиты А, В и С, вирус Эпштейн-Барр, цитомегаловирус, вирус герпеса, ВИЧ, парвовирус В19 и др.).
- гормональные нарушения со стороны яичников, щитовидной шелезы и вилочковой железы.
Некоторые вредоносные агенты непосредственно воздействуют на костный мозг (
ионизирующее излучение, химические и лекарственные вещества). Иные воздействуют опосредованно через аутоиммунные механизмы (
вирусный гепатит В).
Механизм развития апластической анемии
![]()
На сегодняшний день в научном мире существуют несколько теорий, описывающих механизм развития апластической анемии. Занимательно то, что все теории являются полностью доказанными, и, тем не менее, не всегда могут объяснить угнетение костного мозга в том или ином конкретном случае.
Различают следующие теории патогенеза апластической анемии: - стромальная;
- аутоиммунная;
- преждевременный апоптоз.
Стромальная теория
Доказано, что рост и созревание клеток костного мозга невозможен без влияния факторов, вырабатываемых стромой. Строма является скоплением соединительнотканных клеток, образующих своего рода «скелет» или «ложе» в котором залегают клетки костного мозга. Строма вырабатывает такие вещества как ИЛ (
интерлейкины) 1, 3 и 6 и фактор стволовых клеток. Данные вещества направляют развитие клеток предшественников в то или иное русло на различных стадиях их развития.
В 15 – 20% случаев апластических анемий причинной их развития становится недостаточное формирование и выделение стромальных факторов роста. По этой причине дифференцировка клеток крови останавливается на определенной стадии развития. В костном мозге при специальном исследовании можно обнаружить скопление предшественников клеток крови. В периферической крови отмечается увеличение эритропоэтина, который в норме влияет на строму костного мозга.
Аутоиммунная теория
В биоптатах костного мозга в большинстве случаев обнаруживаются очаги скопления клеток Т-киллеров,
моноцитов, фактора некроза опухолей альфа и гамма-интерферонов, указывающих на воспалительный механизм развития апластических анемий. При более детальном изучении клеток костномозговых ростков было обнаружено отсутствие на их поверхности определенного белково-углеводного комплекса, кодируемого геном PIG-A. Мутация данного гена приводит к отсутствию синтеза вышеуказанного комплекса. Вследствие этого не происходит инактивации системы комплемента – одного их звеньев иммунной защиты организма. В результате
иммунитет воспринимает собственные клетки как чужеродные и стремится их уничтожить. Чем больше популяция мутировавших клеток по отношению к здоровым, тем более выражено нарушение синтеза клеток костного мозга.
Теория преждевременного апоптоза
Апоптоз является физиологическим процессом, при котором происходит самостоятельное разрушение клеток с определенными мутационными аномалиями или клеток, изживших отведенный им срок. Посредством апоптоза организм защищается от накопления мутаций и вызванных этим осложнений преимущественно опухолевого происхождения. Однако апоптоз может стать и патологическим процессом, когда будет приводить к преждевременному саморазрушению клеток. Причина преждевременного апоптоза заключается в мутации гена, синтезирующего белок Р-450.
Несмотря на существование нескольких успешных теорий развития апластических анемий, в научном мире по-прежнему ведутся многочисленные исследования в данном направлении. Однако для практикующего врача, и тем более для пациента, поиск механизма, по которому происходит развитие заболевания, практически никогда не имеет смысла. Это связано с тем, что на сегодняшний день не существует более или менее эффективных препаратов, помимо стероидных гормонов, способных замедлить прогрессию анемии или хотя бы частично ее компенсировать. К тому же, наиболее эффективным лечением сегодня является трансплантация костного мозга. Поэтому изучение механизма развития апластической анемии имеет исключительно научный интерес.
Симптомы апластической анемии
![]() Классические симптомы апластической анемии вписываются в следующие синдромы:
Классические симптомы апластической анемии вписываются в следующие синдромы: - анемический;
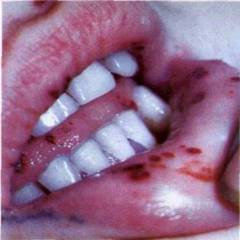
- геморрагический;
- токсико-инфекционный.
Анемический синдром проявляется: - смешанной одышкой, возникающей при умеренной и незначительной физической нагрузке;
- повышенной утомляемостью;
- потемнением и мушками перед глазами;
- головокружением;
- тошнотой;
- тахикардией и аритмиями;
- появлением систолических анемических сердечных шумов и др.
Геморрагический синдром проявляется: Токсико-инфекционный синдром проявляется: - слабым иммунным статусом организма;
- тяжелым течением легких вирусных заболеваний;
- медленным заживлением ран;
- нагноением царапин и др.
Отдельного внимания заслуживают врожденные формы апластических анемий, поскольку обладают некоторыми особенностями, позволяющими в раннем возрасте заподозрить данное заболевание и по мере возможности повлиять на его течение.
Анемия Фанкони
Редкая врожденная апластическая анемия с тяжелым течением, диагностируемая в возрасте от 4 до 10 лет. Поражает с одинаковой частотой мужской и женский пол. Развивается по причине высокой подверженности ДНК клеток тела, и костного мозга в частности, к различного рода мутациям. Клинически проявляется тремя вышеперечисленными синдромами. Степень выраженности симптомов болезни имеет волнообразный характер с периодами ремиссий и обострений. Отмечается высокий риск развития злокачественных опухолевых процессов.
До 80% больных рождаются со следующими телесными аномалиями: - Со стороны мышечно-костной системы - добавочные, отсутствующие или сращенные пальцы, недоразвитие или отсутствие лопаток, незаращение твердого неба (волчья пасть, заячья губа), отсутствие ушных раковин, деформация хрящей носа, добавочные позвонки, сколиоз и др.
- Со стороны нервной системы - микроэнцефалия или анэнцефалия, макроцефалия, спинномозговые грыжи, слепота, глухота, миастения, парапарезы и тетрапарезы, умственная отсталость.
- Со стороны мочеполовой системы - недоразвитие или отсутствие почек, добавочные почки, почечный поликистоз, S-образная почка, подковообразная почка (сращение одного из полюсов) эктопия мочеточников, экстрофия (выворот) мочевого пузыря, агенезия (отсутствие развития) матки, двурогая матка, полное заращение девственной плевы, анорхия (отсутствие яичек), агенезия уретры и пениса и др.
- Со стороны сердечно-сосудистой системы - незаращение овального отверстия и межпредсердной перегородки, открытый баталов проток, стенозы аорты на различных уровнях, инверсия магистральных сосудов сердца и др.
- Со стороны пищеварительной системы - стенозы и аневризмы кишечника, дивертикулез, атрезия кишечника (слепо заканчивающийся кишечник), бронхопищеводные свищи на различных уровнях.
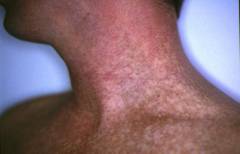
У 75% пациентов наблюдается
кожа оттенка кофе с молоком. Встречаются и витилиго – участки кожи с увеличенной или уменьшенной пигментацией. Единственным способом поддержания жизни больного является переливание недостающих компонентов крови. По этой причине через 4 – 5 лет болезни кожа пациентов приобретает сероватый оттенок из-за избытка железа при разрушении эритроцитов. В случаях, когда врожденные аномалии совместимы с жизнью, в качестве лечения допускается пересадка костного мозга. Тем не менее, прогноз заболевания неблагоприятный. Большинство пациентов умирают в среднем в возраст 7 лет.
Анемия Даймонда-Блекфена
Данный тип анемии считается парциально пластическим, поскольку проявляется угнетением исключительно эритроцитарного ростка костного мозга без вовлечения лейкоцитарного и тромбоцитарного ростков. Заболевание носит семейный характер и может проявиться, если хотя бы один родитель болен им. Поскольку заболевание является аутосомно-доминантным, то вероятность проявления колеблется в пределах 50 – 100% в зависимости от комбинации генов родителей.
Непосредственная причина заболевания – низкая чувствительность клеток костного мозга к эритропоэтину. Клинически наблюдается только анемический синдром. Замечена высокая вероятность развития острых
лейкозов. В большинстве случаев определяются антитела к эритрокариоцитам, поэтому часто эффективным оказывается иммуносупрессивное лечение. Поддерживающее лечение осуществляется посредством регулярных переливаний эритроцитарной массы.
Диагностика апластической анемии
![]()
Клиническая картина заболевания может в значительной степени ориентировать врача в направлении анемии, однако диагноз должен быть подтвержден или опровергнут при помощи лабораторных анализов и параклинических исследований.
Наиболее ценными дополнительными исследованиями являются: Общий анализ крови
Данные общего анализа крови при апластической анемии свидетельствуют в пользу панцитопении (
снижение количества всех трех типов клеток костного мозга). Уменьшение количества лейкоцитов наблюдается преимущественно за счет снижения гранулоцитов (
нейтрофилы, эозинофилы и базофилы). Таким образом, относительно увеличивается процент лимфоцитов и моноцитов в лейкоцитарной формуле. На различных стадиях заболевания могут быть выявлены воспалительные признаки в той или иной мере.
Ориентировочными показателями ОАК при апластической анемии являются: - Гемоглобин (Hb) – менее 110 г\л (норма 120 – 160 г\л). Уменьшение за счет снижения числа эритроцитов.
- Эритроциты – 0,7 – 2,5 х 1012\л (норма 3,7 х 1012\л). Снижение количества зрелых эритроцитов.
- Ретикулоциты - менее 0,2% (норма 0,3 – 2,0%). Снижение количества молодых форм эритроцитов.
- Цветовой показатель – 0,85 – 1,05 (норма 0,85 – 1,05) свидетельствует о нормохромном характере анемии (содержание гемоглобина в эритроците в пределах нормы).
- Гематокрит (Ht) – менее 30 (норма 35 – 42 у женщин и 40 – 46 у мужчин). Соотношение клеточного состава крови к ее жидкой части. Наблюдается явное уменьшение доли клеток в периферической крови.
- Тромбоциты – менее 35 промилле или 100 х 109\л. Снижение количества тромбоцитов.
- Лейкоциты – 0,5 – 2,5 х 109\л (норма 4 – 9 х 109\л). Выраженная лейкопения за счет снижения числа гранулоцитов (нейтрофилы, эозинофилы и базофилы).
- Палочкоядерные нейтрофилы – 0 – 2% (норма менее 6%). Снижение выработки молодых форм лейкоцитов.
- Сегментоядерные нейтрофилы – 0 – 40% (норма 47 – 72%). Снижение количества зрелых форм нейтрофилов.
- Миелоциты – 0 – 2% (в норме отсутствуют). В условиях гранулоцитопении и наслоения бактериальной инфекции наблюдается более выраженный, чем обычно, сдвиг лейкоцитарной формулы влево с появлением клеток предшественников лейкопоэза.
- Эозинофилы – 0 – 1% (норма 1 – 5%). Снижение количества эозинофилов.
- Базофилы – 0% (норма 0 – 1%). Единичные или полное отсутствие базофилов.
- Лимфоциты – более 40% (норма 19 – 37%). Численное количество лимфоцитов остается в норме. За счет снижения фракции гранулоцитов наблюдается относительный лимфоцитоз (увеличение доли лимфоцитов в крови). Крайне выраженный лимфоцитоз может наблюдаться при наслоении вирусных инфекций.
- Моноциты – более 8% (норма 6 – 8%). Количество моноцитов неизменно и находится в пределах нормы. Моноцитоз (увеличение доли моноцитов в крови) объясняется снижением процентной доли гранулоцитов в лейкоцитарной формуле.
- Скорость оседания эритроцитов – более 15 – 20 мм\час (норма до 10 мм/час у мужчин и до 15 мм/час у женщин). Данный показатель отражает степень выраженности воспалительной реакции в организме.
- Анизоцитоз – наличие в крови эритроцитов различного размера.
- Пойкилоцитоз – наличие в крови эритроцитов различной формы.
Биохимический анализ крови
Некоторые виды биохимических анализов крови могут акцентировать внимание врача на отклонениях в организме, которые косвенно вписываются в три вышеперечисленных анемических синдрома.
Ориентировочными показателями БАК при апластической анемии являются: - Сывороточное железо более 30 мкмоль\л (норма 9 – 30 мкмоль/л). Увеличение сывороточного железа на фоне частых переливаний крови. Высокий риск развития гемохроматоза.
- Эритропоэтин более 30 МЕ\л (норма 8 – 30 МЕ/л у женщин и 9 – 28 МЕ\л у мужчин). Увеличение эритропоэтина происходит по двум причинам. Во-первых, не происходит его потребления клетками эритроцитарного ростка. Во-вторых, компенсаторно усиливается его синтез в ответ на анемию.
- НBs-АГ и анти HBcor иммуноглобулины G – положительны (в норме - отрицательны). Данный анализ указывает на наличие вирусного гепатита В. В ряде случаев данный вирус провоцирует развитие аутоиммунной реакции против клеток костного мозга.
- С-реактивный белок – более 10 – 15 мг\л (норма 0 – 5 мг\л). Выявляется при воспалительной реакции на фоне ослабленного иммунитета.
- Тимоловая проба – более 4 (норма 0 - 4). Выявляет признаки воспаления при ослабленном иммунитете.
Стернальная пункция
Данный вид исследования используется с целью визуализации клеток костного мозга и их процентного соотношения. Пункция осуществляется в процедурном кабинете с применением стерильного инструментария и
обезболивающих препаратов, преимущественно ингаляторного действия. Обработка места прокола осуществляется попеременно несколькими антисептическими растворами. Пациент находится в положении лежа на спине. Для пункции используются специальные широкие иглы с ограничителем глубины ввода. Шприц и поршень должны обеспечивать достаточный уровень компрессии, поэтому предпочтительнее использовать стеклянные шприцы с железным поршнем. Классически прокол осуществляется в теле грудины на уровне 2 – 3 ребра медленными вращательными движениями до ощущения провала. Резкое прободение повышает риск соскальзывания иглы с грудины и ранение органов грудной полости. После ощущения провала игла фиксируется одной рукой, а второй рукой производится тракция стержня шприца. Забор пунктата осуществляется до отметки 0,3 – 0,5 мм, после чего иглу извлекают, а отверстие заклеивают лейкопластырем. При отсутствии пунктата в месте прокола пункцию выполняют повторно на несколько сантиметров ниже. После пункции пациент должен продолжать находиться в горизонтальном положении под наблюдением медицинского персонала еще в течение 30 минут.
После извлечения шприца выполняется его опорожнение на несколько предметных стекол, из которых впоследствии будут изготовлены 10 – 15 мазков. Мазки фиксируются, окрашиваются и исследуются согласно соответствующим методикам. Результат исследования именуется миелограммой. Миелограмма отражает фактический и относительный клеточный состав костного мозга.
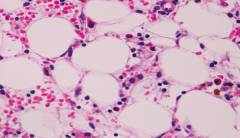
При апластической анемии миелограмма будет скудной, количество клеточных элементов значительно снижено. Камбиальные клетки эритроцитарного и лейкоцитарного ряда единичны или отсутствуют. Мегакариобласты отсутствуют. В редких случаях при пункции случается встретить сгруппированные очаги повышенной пролиферации клеток как компенсаторную реакцию здорового костного мозга на анемию. Такая миелограмма может сбить с толку, поскольку будет свидетельствовать в пользу отсутствия апластической анемии и поэтому будет ложноотрицательной.
Трепанобиопсия
Трепанобиопсия является способом изъятия части костного мозга из крыла подвздошной кости пациента. Преимущество данной процедуры над стернальной пункцией заключается в возможности забора большего количества материала с сохранением его структуры. Большее количество материала уменьшает вероятность ложноотрицательного результата апластической анемии, а изучение структуры костного мозга позволяет помимо цитологического исследования (
миелограммы) провести еще и гистологическое.
При трепанобиопсии пациент находится в положении лежа на животе. Иглы для проведения данной процедуры схожи с иглами при стернальной пункции, но больше в размерах. Обезболивание и техника забора материала идентична вышеописанной. Результаты трепанобиопсии повторяют результаты стернальной пункции. Вдобавок к этому определяется увеличение процентной доли стромы по отношению к кроветворным клеткам, а также увеличение доли желтого неактивного костного мозга по отношению к красному активному.
При помощи анализа крови и результатов трепанобиопсии возможно определение степени тяжести апластической анемии.
Апластическая анемия средней тяжести определяется следующими показателями: - гранулоциты менее 2,0 х 109\л;
- тромбоциты менее 100 х 109\л;
- ретикулоциты менее 2 – 3%;
- гипоплазия костного мозга на трепанобиопсии.
Апластическая анемия тяжелой степени определяется следующими показателями: - гранулоциты менее 0,5 х 109\л;
- тромбоциты менее 20 х 109\л;
- ретикулоциты менее 1%;
- аплазия костного мозга на трепанобиопсии.
Апластическая анемия крайне тяжелой степени определяется следующими показателями: - гранулоциты менее 0,2 х 109\л;
- тромбоциты единичные или отсутствуют;
- ретикулоциты единичные или отсутствуют;
- аплазия костного мозга на трепанобиопсии.
Лечение апластической анемии медикаментами
![]()
Лечение апластической анемии является сложным и комплексным процессом. В начальных стадиях заболевания применяются различные курсы терапии глюкокортикоидными гормонами и цитостатиками с целью снижения иммунной реактивности организма. В большинстве случаев подобный подход дает временные положительные результаты, поскольку механизм развития апластической анемии во многом связан с аутоиммунными реакциями.
Медикаменты являются неотъемлемой частью лечения апластической анемии. Наиболее часто используются три группы препаратов - иммунодепрессанты (
дексаметазон, метилпреднизолон и др.), цитостатики (
циклофосфан, 6-меркаптопурил, циклоспорин А, метотрексат, имуран и др.) и
антибиотики (
цефалоспорины, макролиды, азалиды, хлорхинолоны и др.). Реже могут использоваться препараты для коррекции
артериального давления, нарушений перистальтики
микрофлоры кишечника, ферментные препараты и др.
Иммуносупрессоры могут быть использованы в виде монотерапии лишь в начальных стадиях заболевания и в процессе диагностики. Цитостатики при апластической анемии могут применяться в комбинации с иммуносупрессорами. Также важным их предназначением является очистка концентрата стволовых клеток от примесей злокачественных клеток. Антибиотики применяются во всех стадиях заболевания с целью лечения сопутствующих инфекционных осложнений, возникающих на фоне ослабленного или даже отсутствующего иммунитета.
Операция при апластической анемии
По мере прогрессирования панцитопении возникает необходимость в трансплантации костного мозга – единственного радикального способа излечения апластической анемии. Проблема заключается в том, что для пересадки необходим донор, который предоставит костный мозг совместимый или хотя бы частично совместимый по антигенному составу с костным мозгом реципиента. Нахождение донора может занять длительное время, которым больной в большинстве случаев не располагает. В таких случаях пациенту осуществляются переливания цельной донорской крови или ее компонентов с целью поддержания компенсированного состояния его здоровья.
В данном разделе необходимо указать, что операция, как таковая, производится только донору костного мозга. Реципиент не оперируется. На протяжении десятилетий с момента первой трансплантации костного мозга в 1968 году изучались различные способы введения в организм больного стволовых клеток. Из всех методов наиболее эффективным оказалось внутривенное их введение. Именно по этой причине в дальнейшем операция при апластической анемии будет именоваться трансплантацией стволовых клеток.
Существуют следующие виды трансплантации стволовых клеток: - аллогенная трансплантация костного мозга;
- аллогенная трансплантация периферических стволовых клеток крови;
- аутологичная трансплантация пуповинной крови;
- аутологичная трансплантация костного мозга;
- аутологичная трансплантация периферических стволовых клеток крови;
- сингенная трансплантация костного мозга.
Аллогенная трансплантация костного мозга
Данный вид лечения подразумевает извлечение костного мозга донора и трансплантацию его больному реципиенту. Выполнение данной процедуры является технически сложным процессом и подразумевает соблюдение определенных правил.
В первую очередь донор должен быть совместим с организмом реципиента по трем антигенам в двух комплексах гистосовместимости HLA. В итоге ожидается полное сходство донора и реципиента по 6 антигенам. Минимальным порогом, при котором может осуществиться трансплантация является совпадение по 4 из 6 антигенов, однако в этом случае риски различного рода осложнений возрастают в несколько раз. По приблизительным подсчетам только в 30% случаев среди ближайших родственников больного отыскиваются доноры, полностью совместимые по всем 6 антигенам. Не имеет значения ни возраст, ни пол донора. Самым молодым донором в мире являлся четырехмесячный ребенок с весом тела 3,6 кг.
Операция по извлечению костного мозга является модификацией трепанобиопсии с некоторыми изменениями. В первую очередь данное вмешательство значительно более болезненно, поэтому обязательно использование общей или
эпидуральной анестезии. Использующиеся иглы обладают большим диаметром. Пункция выполняется от 10 до 20 раз в гребешок каждой подвздошной кости. Количество забираемого материала значительно выше и составляет 10 – 15 мл на килограмм массы тела донора. Таким образом, у донора весом 70 кг будет взято количество костного мозга равное 700 – 1050 мл. Осложнения после подобной процедуры развиваются менее чем в 1% случаев. Подавляющее большинство осложнений связано с анестезией и острой
сердечной недостаточностью при массивной кровопотере.
В дальнейшем полученный костный мозг медленно переливается в организм реципиента при помощи внутривенного доступа. Однако подобные случаи достаточно редки, и чаще костный мозг получается из специальных банков-хранилищ биологических материалов. Данные банки пополняются донорами по всему миру. На сегодняшний день насчитывается более 50 национальных банков-хранилищ биологических материалов и более 4 миллионов доноров по всему миру. После выделения костного мозга его необходимо сохранить на длительное время. Для этого он помещается в специальный раствор, не образующий кристаллов льда при замораживании и размораживании. Темпы охлаждения равняются 3 градусам в минуту. При температуре -85 градусов стволовые клетки сохраняются в течение 6 месяцев. При температуре -196 градусов стволовые клетки сохраняются в течение десятков лет. При необходимости использования стволовые клетки размораживаются при температуре 44 – 45 градусов.
Перед введением взвеси стволовых клеток производится их обработка цитостатиками с целью уничтожения примеси злокачественных клеток. Длительный период после трансплантации пациент должен получать интенсивную иммуносупрессивную терапию с целью предотвращения отторжения трансплантата и других нежелательных иммунных реакций.
Аллогенная трансплантация периферических стволовых клеток крови
Несмотря на то, что наиболее распространенным способом добывания стволовых клеток из организма донора является вышеописанная операция, в последние годы активно исследуется метод получения стволовых клеток из периферической крови. Его суть заключается в отделении определенный видов клеток при помощи физического явления, называемого лейкаферезом, с последующей фильтрацией крови в специальных клеточных сепараторах. В данном случае источником стволовых клеток является донорская кровь. После извлечения она обогащается рекомбинантными факторами роста, что приводит к ускорению темпов деления стволовых клеток и увеличению их количества.
Такой метод имеет ряд преимуществ. Во-первых, его побочные эффекты такие же, как при обычном заборе донорской крови. Во-вторых, не страдает костный мозг донора, который при операции должен восстанавливаться в течение как минимум полугода. В-третьих, после трансплантации добытых таким образом стволовых клеток реже развиваются побочные иммунные реакции.
Аутологичная трансплантация пуповинной крови
В некоторых роддомах в последние годы появилась возможность сохранения пуповинной крови, извлеченной из плаценты непосредственно после
родов и перевязывания пуповины ребенка. Такая кровь крайне богата стволовыми клетками. Консервация пуповинной крови производится таким же образом, как описано выше, и хранится в течение многих лет в банках-хранилищах биологических материалов. Сохранение крови производится на случай возникновения у ее хозяина заболеваний крови в будущем, в том числе и апластической анемии. Стволовые клетки, полученные из такой крови, не вызывают реакции отторжения трансплантата и находятся в скором доступе. Недостаток подобных услуг заключается только в высокой стоимости, поскольку содержание ячейки в подобном банке на сегодняшний день по силам только людям с достатком гораздо выше среднего уровня.
Аутологичная трансплантация костного мозга
Данный способ подразумевает изъятие костного мозга у пациента до заболевания крови или в момент полной клинической ремиссии с целью дальнейшего его использования при появлении необходимости. Хранение костного мозга осуществляется аналогичным образом. Конфликт несовместимости стволовых клеток донора и реципиента исключается, поскольку донор и реципиент является одной и той же личностью.
Аутологичная трансплантация периферических стволовых клеток крови
При данном виде трансплантации пациенту пересаживаются стволовые клетки, добытые из его же крови до развития заболевания крови. Конфликт антигенной несовместимости также исключается.
Сингенная трансплантация костного мозга
Трансплантация стволовых клеток производится от донора, которым является гомозиготный (
однояйцевый) близнец больного. Антигены на поверхности клеток их организмов идентичны, поэтому такой трансплантат не вызовет реакции отторжения и приравнивается к аутологичному.
После проведенной пересадки стволовых клеток пациент должен находиться под бдительным контролем медицинского персонала. Обязательно проведение активной иммуносупрессивной терапии. Низкий иммунитет больного подразумевает его нахождение в специализированных стерильных палатах с замкнутой системой вентиляции, бактериальными фильтрами и т. п. Перед тем как войти в палату медицинский персонал должен быть одет в стерильные костюмы и пройти через санпропускник.
Осложнения трансплантации костного мозга
Осложнения трансплантации костного мозга разделяются на следующие группы: - инфекционные осложнения;
- реакция «трансплантат против организма хозяина»;
- реакция отторжения трансплантата;
- отказ жизненно важных органов.
Инфекционные осложнения
Развитие осложнений такого рода характерно как для донора костного мозга, так и для пациента, которому он пересаживается. Нагноение послеоперационной раны у доноров развивается достаточно редко ввиду небольшого размера пункционных отверстий. Тем не менее, при попадании в них анаэробных бактерий существует риск развития тяжелого вторичного
остеомиелита. Инфекционные осложнения у реципиента костного мозга происходят по причине интенсивной иммуносупрессии, производящейся с целью успешного приживления стволовых клеток. На фоне снижения иммунитета присоединяются различные бактериальные инфекции, которые должны быть лечены высокими дозами антибиотиков широкого спектра.
Реакция «трансплантат против организма хозяина»
Суть данного осложнения заключается в конфликте иммунных клеток организма хозяина со свежесформированными иммунными клетками донорских стволовых клеток. При этом донорские лимфоциты проявляют выраженную агрессию по отношению к лимфоцитам хозяина. Клинически это проявляется обильной
сыпью, кожными буллами, язвами, нарушением функций желудочно-кишечного тракта, сердечно-сосудистой системы и т. д.
Данное осложнение развивается исключительно при пересадке костного мозга или стволовых клеток от аллогенного донора. При пересадке собственных, замороженных ранее стволовых клеток, такое осложнение не развивается. Данное осложнение происходит при полной совместимости костного мозга донора и реципиента по всем 6 антигенам в 30% случаев. При частичной совместимости риск такого осложнения возрастает до 80%. С целью профилактики данной патологической реакции применяются цитостатики. Наиболее часто препаратом выбора является циклоспорин А в паре с одним из следующих препаратов - метотрексат, имуран или глюкокортикоиды (
дексаметазон, метилпреднизолон и др.)
Реакция отторжения трансплантата
Данное осложнение развивается, когда иммунная система организма хозяина определяет донорские стволовые клетки как угрозу и стремится их уничтожить. Оно характерно при пересадке донорских стволовых клеток. При пересадке собственных клеток такое осложнение исключается. У больных с апластической анемией реакция отторжения трансплантата развивается в 20% случаев, то есть у каждого пятого пациента. При подозрении на данный процесс вдобавок к кортикостероидам назначаются рекомбинантные факторы роста, увеличивающие темпы сращения тканей.
Отказ жизненно важных органов
Трансплантация костного мозга является тяжелым испытанием для всех органов и систем организма. Высокие дозы медикаментов, в частности цитостатиков, оказывают разрушительное действие на ткани печени, почек, эндокринных желез и др. При истощении защитных резервов органов прекращается их функционирование. Наиболее часто наблюдается развитие острой
печеночной недостаточности и
почечной недостаточности. Драматизм такого осложнения заключается в том, что в большинстве случаев единственным методом лечения является пересадка пораженных органов от доноров. Но ввиду того, что причина отказа органов не устранена, пересадку здорового органа осуществлять нельзя, так как он через короткое время таким же образом выйдет из строя.
Прогноз при апластической анемии
![]()
Прогноз при апластической анемии во многом зависит от сроков обнаружения заболевания. При раннем обнаружении существует возможность более активного вмешательства в течение заболевания. При более позднем обнаружении шансы на излечение уменьшаются.
Врожденная апластическая анемия Фанкони в большинстве случаев крайне тяжело поддается лечению, поскольку костный мозг никогда не был здоровым и, соответственно, очень сложно восстанавливается. Наличие врожденных аномалий развития сильно ограничивает показания к пересадке костного мозга таким пациентам. В большинстве случаев больные погибают в детском возрасте от аномалий развития или инфекционных осложнений.
Приобретенные апластические анемии имеют более благоприятный прогноз, поскольку в некоторых случаях являются обратимыми после прекращения действия повреждающего фактора на костный мозг.
Применение методов консервации пуповинной крови, стволовых клеток костного мозга и периферической крови повышает шансы на полное выздоровление до 75 – 80%.