Содержание статьи:
Бактериофаги – вирусы заражающие бактерии – вошли в медицину двумя путями: прямым и окольным. Прямой известен многим: еще в начале прошлого столетия фаги начали использовать для борьбы с бактериальными инфекциями. Окольный путь проходит через микробиологию, и здесь преимущества бактериофагов раскрываются в полную силу только сейчас.
Вирусы бактерий интересовали молекулярных биологов всегда. Фаги устроены очень просто, поэтому на них удобно изучать работу ДНК, и они не опасны для человека. Например, фаг лямбда, заражающий кишечную палочку, надолго стал «рабочей лошадкой» ученых. На нем были открыты многие фундаментальные биологические процессы.
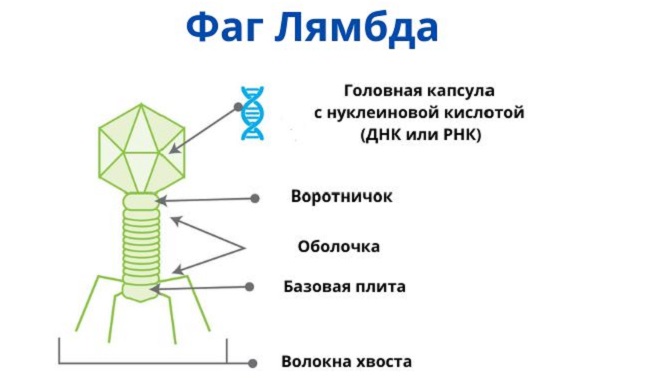
Фаг лямбда – незаменимый помощник ученых, занимающихся молекулярной биологией и генетикой. © goldbio.com
Современные технологии позволяют не только изучать фаги, но и создавать с помощью них медикаментозные препараты. Особенно интересны «фаговые» антитела и вакцины. О них и поговорим. Но начнем с небольшой предыстории.
Краткая история антител в медицине: от открытия до полномасштабного производства
Антитела, они же иммуноглобулины – особые белковые молекулы, которые обеспечивают защиту организма от возбудителей инфекций и собственных «неправильных» клеток. Считается, что только они, среди всех защитных механизмов нашего тела, способны полностью побеждать инфекции. Они работают и на профилактику, и на борьбу с уже возникшим заболеванием.
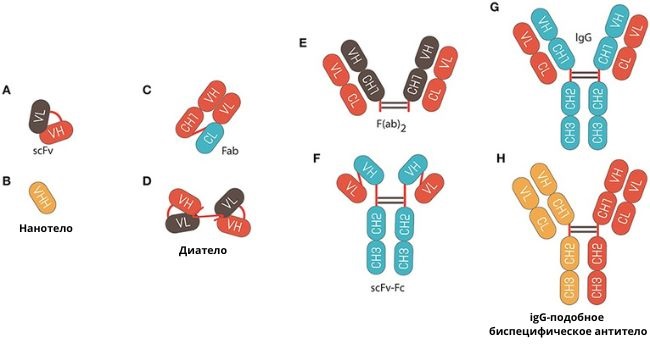
Схематическое изображение разных типов молекул антител. © frontiersin.org
Иммуноглобулины впервые были обнаружены в конце XIX столетия, когда ученые заметили, что перенос антител от зараженного животного здоровому защищает от дифтерии. Появилось даже такое направление в лечении инфекций – сывороточная терапия. В качестве лекарства выступали сыворотки иммунизированных животных. Но их быстро вытеснили антибиотики, оказавшиеся более эффективными, безопасными и дешевыми в производстве.
Вскоре ученые поняли, почему антитела так эффективно работают: их молекулы устроены так, что они могут распознавать определенные вещества и нацеливать против них иммунную систему. Это свойство оказалось очень полезным: за счет него антитела можно использовать, чтобы выявлять определенные вещества во время лабораторных анализов и блокировать определенные молекулы в организме человека, которые вызывают болезни. Дело оставалось за малым: научиться производить иммуноглобулины, направленные против нужных антигенов, в товарных количествах.
В 1975 году ученые Колер и Мильштейн придумали технологию создания моноклональных антител, то есть таких, которые произведены одним клоном иммунных клеток и направлены против одного антигена. Суть метода:
- Животным вводят антиген, чтобы их иммунные клетки начали вырабатывать нужные антитела.
- Нужные иммунные клетки выделяют из крови животного.
- Затем эти иммунные клетки в пробирке «скрещивают» с опухолевыми клетками, чтобы сделать их «бессмертными».
- Клеточный клон производит нужный тип иммуноглобулинов, а ученые используют их для производства лекарственного или диагностического препарата.
В 1980-е годы были разработаны еще более продвинутые методики производства рекомбинантных антител. Помогла в этом генная инженерия. Ученые смогли синтезировать нужные части антител, а потом собирать из них, как из конструктора, иммуноглобулины с нужными свойствами.
Сегодня на основе иммуноглобулинов разработано много разных лекарственных препаратов. Например, моноклональные антитела успешно применяют для лечения онкологических заболеваний.
Чем могут помочь вирусы бактерий: фаговые дисплеи
Одним из эффективных инструментов для производства терапевтических антител оказались…бактериофаги!
Превращать фаговые частицы в фабрики по производству иммуноглобулинов помогает так называемый метод фаговых дисплеев. Его разработал в 1985 году ученый Джордж П. Смит из США, за что позже был номинирован на Нобелевскую премию в области химии.

Джордж П. Смит – создатель метода фаговых дисплеев. © nobelprize.org
Суть методики фаговых дисплеев в следующем:
- В ДНК вируса вставляют нужный ген.
- С этого гена считываются инструкции и синтезируются определенные белки в соответствии с закодированной в гене информацией.
- Данный белок присутствует на внешней оболочке фага в комплексе с другим белком. Его можно обнаружить при помощи химических способов экстрагирования белка. По его способности реагировать с другими реактивами можно точно сказать, какой ген его кодирует.
- С помощью специальных методик ученые могут отсортировывать бактериофаги с необходимыми белками, формировать из них целые библиотеки. Например, при помощи фаговых дисплеев часто выявляют и отсортировывают антитела, направленные против определенных антигенов.

Очень упрощенная схема фагового дисплея. Оранжевым цветом отмечен белок, ген которого искусственно вводят в ДНК вируса. © irbm.com
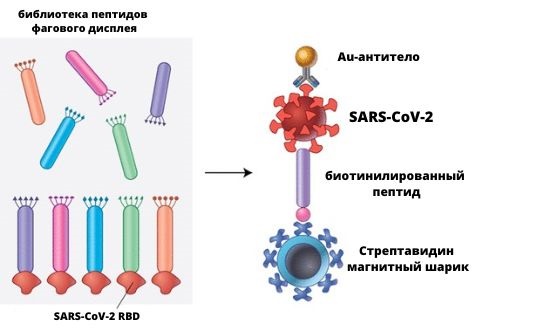
Фаговые дисплеи в деле: пример использования. На рисунке показано, как с помощью библиотеки отбирают фаговые частицы, несущие белок, который специфически связывается с вирусом SARS-CoV-2, вызывающим COVID-19. © pubs.acs.org
Вакцины на основе бактериофагов
Задача вакцинации – ввести в организм человека некое подобие возбудителя инфекции, которое не вызовет заболевание, но запустит иммунную реакцию и поможет создать защиту. Чтобы добиться такого эффекта, производители препаратов для прививок прибегают к разным хитростям. Можно инактивировать возбудителя, как, например, поступают с вирусом гриппа. Можно синтезировать белки вирусной оболочки, которые соберутся в пустой «вирус-зомби» без генетического материала – так производят вакцины против вирусов папилломы человека (ВПЧ). Создатели российской вакцины Спутник V решили действовать по принципу «троянского коня»: они ввели гены коронавируса в аденовирус.
Если эти фокусы возможно проделывать над человеческими вирусами, почему бы таким же способом не приготовить вакцину из бактериофагов? Эта идея родилась в головах ученых в начале 1980-х годов. На сегодняшний день фаговые вакцины уже существуют, они испытаны на животных. Производят их тремя основными способами:
- С помощью метода фаговых дисплеев, о котором мы говорили выше. Можно заставить фаг синтезировать белок опасного патогена, на который реагирует специфический иммунитет, и разместить его на своей поверхностной оболочке.
- ДНК-вакцины: в данном случае в бактериофаг загружен генетический материал патогенного вируса. Фаг доставляет его в клетки человека, и это провоцирует иммунную реакцию.
- Гибридные фаговые вакцины – сочетание двух предыдущих методов. Причем можно поступить еще хитрее: например, загрузить в фаг «враждебную» ДНК, а на его поверхности выставить белки, которые помогут эффективнее доставить ее в определенные клетки человека. За счет этого иммунная реакция усилится.
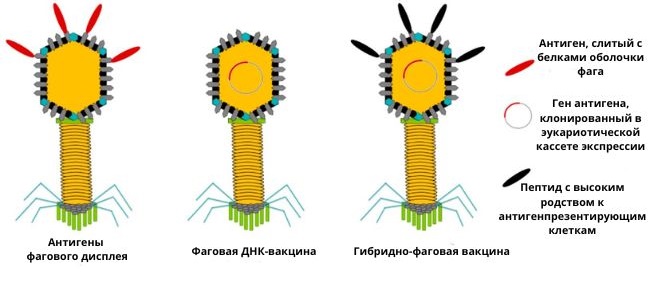
Три способа производства вакцин на основе бактериофагов. © mdpi.com
Например, такая вакцина против COVID-19 на основе фаговых дисплеев была представлена в 2022 году американскими учеными в журнале mBio Американского общества микробиологии. Препарат изготовлен на основе фага T4, его вводят в нос (не нужно делать укол), и он не содержит адъювантов (вспомогательных веществ, усиливающих иммунную реакцию). Новая вакцина обеспечивает надежную защиту от вируса именно там, где она в первую очередь нужна – в дыхательных путях. Испытания показали хороший результат, правда, провели их только на мышах.
Бактериофаги изначально ворвались в медицинскую науку как инструмент для борьбы с бактериальными инфекциями, и долгое время их воспринимали именно в таком амплуа. Сегодня молекулярная биология и генетика открывают множество новых интересных перспектив. И пусть эти перспективы зачастую пока реализованы только «в пробирке» и экспериментах на животных – в будущем данные разработки вполне могут привести к появлению новых методов диагностики, лечения и профилактики болезней.
Список литературы и библиографических ссылок:
- Sciencedirect – Получение человеческих антител с помощью бактериофага
- NCBI – Получение рекомбинантных антител с использованием бактериофагов
- ScienceDaily – Высокоэффективная слизистая вакцина без игл и адъювантов на основе бактериофагов






 Автор на связи, задать вопрос
Автор на связи, задать вопрос