Содержание статьи:
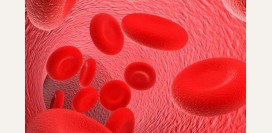
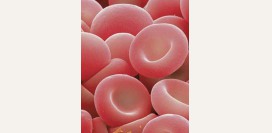
 Талассемия – группа заболеваний крови, характеризующихся генетически обусловленным нарушением образования одной или нескольких цепей гемоглобина в эритроцитах. Это приводит к образованию маленьких, функционально несостоятельных эритроцитов, имеющих форму мишени, что является характерной особенность данного заболевания.
Талассемия – группа заболеваний крови, характеризующихся генетически обусловленным нарушением образования одной или нескольких цепей гемоглобина в эритроцитах. Это приводит к образованию маленьких, функционально несостоятельных эритроцитов, имеющих форму мишени, что является характерной особенность данного заболевания.Основной функцией эритроцитов является доставка кислорода ко всем органам и тканям, причем главную роль в этом процессе играет именно гемоглобин. При талассемии эта функция нарушается, в результате чего все ткани организма начинают испытывать кислородное голодание, что и обуславливает основные клинические проявления заболевания.
Родиной талассемии считаются страны Африки и Юго-Восточной Азии, где частота заболевания составляет от 2 до 25%. Однако на сегодняшний день данный недуг встречается во всех странах мира, что обусловлено, главным образом, высоким уровнем миграции населения. Мужчины и женщины болеют одинаково часто.
Интересные факты
- Талассемия также называется средиземноморской анемией, что связано с высоким уровнем распространенности заболевания в странах средиземноморского бассейна.
- Считается, что высокий уровень талассемии в странах Африки связан с наличием малярии в этой местности.
- Больные некоторыми формами талассемии невосприимчивы к малярии.
- Единственным методом профилактики талассемии является генетическое исследование будущих родителей и эмбриона на ранних стадиях развития.
Что такое эритроциты?
 Эритроцитами называются красные безъядерные клетки крови, которые составляют до 25% от всех клеток организма. Основная роль эритроцитов – транспорт дыхательных газов (кислорода и углекислого газа).
Эритроцитами называются красные безъядерные клетки крови, которые составляют до 25% от всех клеток организма. Основная роль эритроцитов – транспорт дыхательных газов (кислорода и углекислого газа).Образование эритроцитов
Образование эритроцитов (эритропоэз) начинается с 3 недели эмбрионального развития. В зависимости от этапа развития, кроветворение происходит в различных органах.Основными кроветворными органами являются:
- Печень. Первые очаги кроветворения в печени появляются на 6 неделе внутриутробного развития. Начиная с этого периода и до рождения ребенка печень является основным местом образования клеток крови. После рождения кроветворная функция печени угнетается.
- Селезенка. Развитие селезенки начинается на 5 – 6 неделе беременности, однако первые очаги кроветворения в ней появляются на 4 месяце внутриутробного развития. Кроветворная функция селезенки, как и печени, угнетается после рождения ребенка.
- Красный костный мозг (ККМ). Это особое вещество, располагающееся в губчатых костях организма (в костях таза, черепа, позвонках, грудине), а также в длинных трубчатых костях (плеча и предплечья, бедра и голени). Образование эритроцитов в ККМ начинается с 4 месяца беременности. После рождения ребенка, когда кроветворение в печении и селезенке угнетается, красный костный мозг становится единственным кроветворным органом человека.
Из стволовой клетки крови развиваются:
- Эритроциты – обеспечивают транспорт газов в организме.
- Тромбоциты – ответственны за остановку кровотечений.
- Лейкоциты – защищают организм от различных инфекций (бактерий, вирусов и т. д.).
- Лимфоциты – обеспечивают и регулируют защитные функции организма.
Процесс роста и развития эритроцитов контролируется особым веществом – эритропоэтином. Он вырабатывается почками в ответ на гипоксию (недостаток кислорода) и активирует эритропоэз в красном костном мозге. Результатом этого становится ускоренное образование эритроцитов, что приводит к повышению их количества в периферической крови.
В процессе дифференцировки (превращения стволовой клетки в эритроцит), проходящем в красном костном мозге, образуется несколько промежуточных форм клеток (последовательно образуются проэритробласт, эритробласт, нормобласт). Данный процесс длится в среднем 3 суток, в течение которых клетка теряет ядро, органеллы, и накапливает гемоглобин – особое вещество, ответственное за транспорт газов в организме.
Конечным результатом эритропоэза в костном мозге является ретикулоцит (молодая форма эритроцита), который выходит в системный кровоток и в течение суток превращается в зрелый эритроцит.
Зрелый эритроцит окрашен в красный цвет (это обусловлено наличием в нем красного пигмента гема) и имеет форму двояковогнутого диска. Средний диаметр эритроцита составляет 7,5 – 8,3 микрометра.
Образование гемоглобина
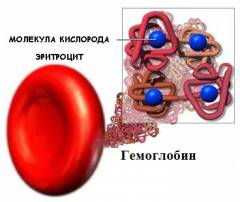
Гемоглобин – особый белково-пигментный комплекс, находящийся в эритроцитах и состоящий на 96% из белка глобина и на 4% из железа. Каждый эритроцит содержит около 300 миллионов молекул гемоглобина (30 пикограмм). Каждая молекула гемоглобина состоит из четырех белковых цепей - а1, а2, b1 и b2. Их образование запрограммировано генетически.Генетический аппарат человека представлен 23 парами хромосом – особых структур, заключенных в ядре клетки и состоящих из ДНК (дезоксирибонуклеиновой кислоты). Каждая хромосома содержит множество генов, а каждый ген, в свою очередь, ответственен за образование определенного вещества в клетке.
Синтез а-цепей глобина контролируется четырьмя генами (по 2 от каждого родителя), расположенными в 16 паре хромосом. Синтез b-цепей контролируется только двумя генами (по 1 от каждого родителя), расположенными в 11 паре хромосом. Данный процесс происходит синхронно, что приводит к образованию строго определенного числа как а-, так и b-цепей.
Образовавшиеся цепи глобина соединяются друг с другом в определенной последовательности, после чего к ним присоединяется железо (гем), в результате чего образуется полноценный гемоглобин. На разных периодах развития образуются различные комбинации глобиновых цепей, в соответствии с чем выделяют различные типы гемоглобина.
В зависимости от периодов развития различают:
- Эмбриональный гемоглобин (HbU). Встречается в организме эмбриона с 3 по 10 недели внутриутробного развития.
- Фетальный гемоглобин (HbF). Является основным типом гемоглобина плода. Его количество постепенно уменьшается, и в период рождения составляет только 20% от общего гемоглобина организма. У взрослого человека встречается в незначительных количествах.
- Взрослый гемоглобин (HbA). При рождении ребенка 80% всего гемоглобина представлено HbA, а к возрасту 2 – 3 лет и до конца жизни его доля составляет 98%.
- Малый компонент взрослого гемоглобина (HbA2). Составляет примерно 2% от общего гемоглобина взрослого человека.
Разрушение эритроцитов
Зрелые эритроциты циркулируют в периферической крови около 120 дней. По истечении этого срока эритроцит «стареет», что проявляется нарушением его способности использовать энергию. Результатом данного процесса является истощение энергетических запасов клетки и деформация ее поверхности (на ней образуются многочисленные выступы и выросты).Разрушение красных клеток крови происходит в селезенке. Нормальные эритроциты имеют гладкую поверхность и довольно гибкие, что позволяет им свободно проходить через капилляры селезенки (диаметр которых составляет 2 – 3 микрометра). «Старые» эритроциты лишены такой возможности, так как утратили свою эластичность. В результате они застревают в селезенке и разрушаются специальными клетками – макрофагами.
Процесс разрушения эритроцитов в макрофагах селезенки сопровождается отделением железа от гемоглобина и переносом его в костный мозг, где оно используется для синтеза новых эритроцитов. Оставшийся гемоглобин подвергается дальнейшему превращению в билирубин – пигмент желтого цвета.
В организме билирубин находится в двух формах - в несвязанной и в связанной. Несвязанная форма попадает в кровоток из эритроцитов при их разрушении. В дальнейшем, при прохождении через печень, билирубин захватывается клетками органа, в которых связывается с глюкуроновой кислотой. В результате этого процесса образуется связанная форма билирубина, которая включается в состав желчи и выводится из организма.
Что такое талассемия?
 Талассемия характеризуется нарушением синтеза одной или нескольких глобиновых цепей, в результате чего нарушается процесс образования гемоглобина и функция эритроцитов.
Талассемия характеризуется нарушением синтеза одной или нескольких глобиновых цепей, в результате чего нарушается процесс образования гемоглобина и функция эритроцитов.Виды талассемий
Различают несколько видов талассемии, в зависимости от того, синтез какой из глобиновых цепей нарушен. Это, в свою очередь, определяется хромосомой, в которой расположен мутантный ген.В зависимости расположения генетической мутации различают:
- А-талассемии;
- B-талассемии;
- AB-талассемию.
Характеризуются дефектом одного или нескольких генов, расположенных в 16 паре хромосом и ответственных за синтез а-цепей глобина. При данной форме заболевания b-цепи глобина образуются с нормальной скоростью и в нормальном количестве. Однако синтез a-цепей нарушен, из-за чего невозможно образование нормального глобинового комплекса (состоящего из двух а-цепей и двух b-цепей). Образующийся при этом гемоглобин состоит полностью или почти полностью из b-цепей и не способен транспортировать газы в организме.
В зависимости от количества мутантных генов различают:
- Бессимптомное носительство. Встречается при поражении одного из четырех генов, ответственных за образование а-цепей глобина. Остальные три гена работают нормально, и образующихся а-цепей достаточно для синтеза нормального гемоглобина. Клинические проявления заболевания в данном случае отсутствуют, однако существует небольшая вероятность рождения ребенка с талассемией у такого человека (если второй родитель также будет носителем мутантного гена).
- Малая а-талассемия. Характеризуется дефектом двух генов, кодирующих образование а-цепей глобина. В этом случае а-цепи образуются в недостаточном количестве, поэтому образование нормального гемоглобина ограничено. Клинические проявления слабо выражены и редко требуют медицинского вмешательства, однако риск рождения ребенка с талассемией повышен.
- Гемоглобинопатия Н. Тяжелая форма заболевания, характеризующаяся поражением трех генов из четырех. Цепи а-глобина образуются в незначительных количествах, поэтому почти весь гемоглобин эритроцитов состоит из четырех b-цепей. Заболевание характеризуется длительным и тяжелым течением и без соответствующего лечения быстро приводит к смертельному исходу.
- Внутриутробная водянка. Характеризуется повреждением всех генов, ответственных за образование а-цепей глобина. При данной форме заболевания гибель плода происходит во внутриутробном периоде либо сразу после рождения.
Данная группа заболеваний встречается гораздо чаще, чем а-талассемии. Принцип возникновения такой же, только дефектный ген располагается в 11 паре хромосом, что приводит к уменьшению количества синтезируемых b-глобиновых цепей.
В результате образуется нестабильный гемоглобиновый комплекс, состоящий только из а-цепей. Он быстро подвергается разрушению, что приводит к разрушению содержащих его клеток (эритробластов в красном костном мозге или эритроцитов в периферической крови).
В зависимости от количества мутантных генов различают:
- Большую талассемию (анемию Кули). Тяжелая форма заболевания, характеризующаяся повреждением обоих генов, кодирующих образование b-цепей глобина.
- Промежуточную талассемию. Характеризуется мутацией одного или обоих генов, однако образующихся при этом b-глобиновых цепей достаточно для синтеза определенного количества нормального гемоглобина. Клиническая картина заболевания в данном случае менее выражена.
- Малую b-талассемию. Характеризуется мутацией одного гена, что приводит к незначительному снижению количества образуемых b-цепей глобина. Заболевание протекает без клинических проявлений.
Крайне редкая форма талассемии, при которой нарушается синтез как а-, так и b-цепей глобина. Гемоглобин в эритроцитах не образуется, в результате чего они не способны транспортировать кислород в организме. Данная форма заболевания несовместима с жизнью и характеризуется внутриутробной гибелью плода.
Изменения в организме при талассемии
Независимо от формы и вида талассемии патологические процессы, происходящие в организме человека при данном заболевании, схожи.Патологические процессы при талассемии характеризуются:
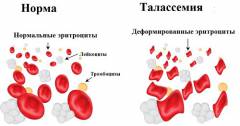
- Нарушением образования эритроцитов. В результате недостаточного количества нормального гемоглобина образуются маленькие эритроциты (менее 7 микрометров в диаметре). Содержащиеся в них цепи глобина расположены в центре клетки и не участвуют в транспорте кислорода.
- Усиленным разрушением эритроцитов. В результате избыточного образования свободных глобиновых цепей (а-цепей при b-талассемии и b-цепей при а-талассемии) происходит их внутриклеточная агрегация (склеивание). Образующиеся комплексы прикрепляются к внутренней поверхности эритроцитов, что приводит к деформации клеток и преждевременному их разрушению (непосредственно в сосудистом русле либо в селезенке).
- Увеличением продукции эритропоэтина почками. Эта компенсаторная реакция организма направлена на устранение гипоксии, которая развивается в результате уменьшения количества нормальных эритроцитов в крови. Эритропоэтин стимулирует разрастание костномозговой ткани в губчатых и трубчатых костях (что приводит к их деформации), а также приводит к появлению экстрамедуллярных (вне костного мозга) очагов кроветворения – в печени и в селезенке.
- Избыточным накоплением железа в организме. В нормальных условиях железо (всасывающееся в кишечнике, либо образующееся в процессе распада эритроцитов) связывается с активными центрами на поверхности трансферрина – особого белка, который осуществляет транспорт данного микроэлемента ко всем органам. Основным органом-депо железа в организме является печень. В клетках печени содержится другое вещество белковой природы – ферритин (в меньших количествах данное вещество содержится в крови, в клетках селезенки, слизистой оболочки тонкого кишечника и плаценты при беременности). Ферритин обладает способностью связывать свободное железо (которое является токсичным для организма) и запасать его в нетоксичной форме. Образование данного белка происходит в печени и контролируется количеством железа в организме - чем его больше, тем больше ферритина синтезируется.
Причины талассемии
 Как говорилось ранее, возникновение талассемии обусловлено генетически. Данное заболевание наследуется по аутосомно-рецессивному типу. Это означает, что у ребенка оно будет проявляться только в том случае, если он унаследует мутантные гены от обоих родителей.
Как говорилось ранее, возникновение талассемии обусловлено генетически. Данное заболевание наследуется по аутосомно-рецессивному типу. Это означает, что у ребенка оно будет проявляться только в том случае, если он унаследует мутантные гены от обоих родителей.Если же ребенок получил только один мутантный ген (только от отца или только от матери), то он может стать носителем данного заболевания. Клинические проявления в этом случае либо вовсе отсутствуют, либо выражены незначительно, однако вероятность того, что его дети будут страдать талассемией, составляет от 25 до 50%.
Выявить первопричину заболевания на сегодняшний день не удалось, несмотря на многочисленные исследования в данной области. Выделяют определенные факторы внешней среды, которые могут способствовать возникновению повреждений на уровне генетического аппарата, однако они неспецифичны и могут вызывать мутации в различных генах, обуславливая появление различных генетических заболеваний.
Факторами, которые могут привести к генетическим мутациям, являются:
- Ионизирующая радиация. Представляет собой поток радиоактивных частиц, которые, проходя через ткани организма, оказывают повреждающее действие на генетический аппарат клеток, что приводит к возникновению множества мутаций. Значение имеет как общий радиационный фон (может быть повышен в зонах взрыва атомных бомб, вблизи аварий на атомных электростанциях), так и интенсивное периодическое воздействие радиации (при частых рентгенологических исследованиях либо при радиотерапии опухолевых заболеваний).
- Химические мутагены. Мутагеном называется вещество, которое при взаимодействии с организмом оказывает влияние на генетический аппарат клеток, способствуя возникновению различных мутаций. Большое количество мутагенов выделяется в различных областях промышленности (при добыче нефти, угля и т. д.) и в повседневной жизни (например, бензол, входящий в состав бензина).
- Лекарственные препараты. В основном противоопухолевые (цитостатические), а также некоторые другие медикаменты (например, колхицин) обладают мутагенной активностью, в связи с чем их применение связано с повышенным риском возникновения различных генетических мутаций.
- Вирусные заболевания. Некоторые вирусы (кори, герпеса, гриппа) могут повлиять на генетический аппарат клеток человека. Вирус представляет собой частицу ДНК. Попадая в клетку, он внедряется в ее гены и изменяет их определенным образом, в результате чего клетка начинает продуцировать копии вируса. Данный процесс может сопровождаться повреждением генетического материала клетки.
- Курение. Табачный дым, вдыхаемый при выкуривании сигареты, содержит множество химических соединений (бензол, фенол и другие), обладающих мутагенной активностью, то есть способных вызывать мутации на уровне генном уровне. Мутагенному воздействию данных веществ подвергается как сам курящий, так и окружающие его люди, вдыхающие табачный дым.
- Алкогольные напитки. Этиловый спирт, входящий в состав алкогольных напитков, снижает устойчивость клеток организма к действию различных мутагенов, повышая риск развития генетических мутаций. Кроме того, длительное применение больших доз алкоголя сопровождается угнетением защитных функций организма (в частности, противоопухолевого иммунитета, ответственного за выявление и разрушение клеток с генетическими мутациями).
Симптомы талассемии
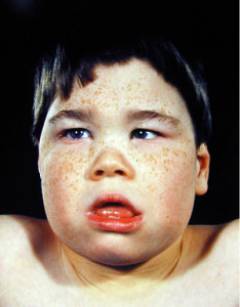 Так как данное заболевание является наследственным, его симптомы начинают проявляться сразу после рождения либо в первые недели жизни ребенка. Клинические проявления схожи при всех видах талассемии – различается только их выраженность, в зависимости от степени нарушения образования гемоглобина.
Так как данное заболевание является наследственным, его симптомы начинают проявляться сразу после рождения либо в первые недели жизни ребенка. Клинические проявления схожи при всех видах талассемии – различается только их выраженность, в зависимости от степени нарушения образования гемоглобина.Основные проявления талассемии обусловлены:
- нарушением образования эритроцитов;
- избыточным кроветворением в красном костном мозге;
- избытком железа в организме;
- усиленным разрушением эритроцитов.
Симптомы нарушения образования эритроцитов
Ввиду того, что синтез гемоглобина в эритроцитах нарушен, они неспособны выполнять свою основную функцию – доставлять кислород к тканям организма. Кроме того, часть эритроцитов разрушается еще до выхода из костного мозга (на стадии эритробласта), что обуславливает уменьшение их количества в крови. Развивается хроническая анемия – состояние, проявляющееся недостатком эритроцитов и гемоглобина в периферической крови.Основными симптомами нарушения образования эритроцитов являются:
- Бледность кожных покровов. Розоватую окраску коже и слизистым оболочкам придают эритроциты, так как они содержат красного цвета гемоглобин. Из-за недостаточного количества эритроцитов кожа становится бледной, сухой, нарушается ее эластичность.
- Слабость и повышенная утомляемость. Данные симптомы обусловлены длительным недостатком кислорода в организме. Отмечается вялость, апатия (отсутствие настроения и инициативы), малоподвижный образ жизни.
- Снижение концентрации внимания. Из-за недостаточного поступления кислорода к головному мозгу нарушаются его функции. В частности, дети с талассемией начинают говорить позже сверстников, могут отставать в умственном развитии, хуже учатся в школе.
- Замедление роста. Рост и развитие всех тканей организма напрямую зависит от достаточного поступления кислорода к ним. При его недостатке нарушаются процессы клеточного деления, что приводит к замедлению роста и нарушению работы всех органов. При талассемии отмечается низкий рост, маленькая масса тела (по отношению к возрастной группе), снижение аппетита.
- Непереносимость физических нагрузок. Процессы мышечного сокращения требуют постоянного наличия энергии, что обеспечивается только при достаточном количестве кислорода в мышцах. Запасы энергии в мышцах крайне малы, поэтому нарушение доставка кислорода довольно быстро приводит к их истощению. Это проявляется мышечной слабостью, дети малоактивны, предпочитают «сидячие» игры. При физических нагрузках отмечается быстрая утомляемость, может развиваться чувство нехватки воздуха, усиленное и учащенное сердцебиение. Данные симптомы исчезают или ослабевают после нескольких минут отдыха, однако при возобновлении физической активности вновь появляются.
- Язвы кожных покровов. Данный симптом характерен для тяжелых форм заболевания, характеризующихся значительным дефицитом эритроцитов и гемоглобина в крови. В этом случае доставка кислорода нарушена настолько сильно, что в различных органах и тканях развиваются дистрофические изменения. Наиболее часто язвы образуются в области ног и рук, так как они расположены наиболее далеко от сердца и легких, и к ним поступает меньше всего кислорода, что приводит к нарушению питания кожных покровов и мягких тканей. Пораженный участок кожи становится чувствительным к незначительным травмам и инфекциям, результатом которых часто становится изъязвление (образуются так называемые трофические язвы). Реже трофические язвы поражают другие участки тела.
- Увеличение печени и селезенки. Из-за недостатка кислорода в организме активируются различные компенсаторные механизмы, одним из которых является появление очагов кроветворения вне костного мозга - в печени и в селезенке. Данные органы увеличиваются в размерах, становятся более плотными. Дети жалуются на тяжесть и/или болезненность в правом подреберье, отмечается нарушение пищеварения.
Симптомы избыточного кроветворения в красном костном мозге
Как говорилось ранее, недостаток кислорода приводит к повышенной выработке почками эритропоэтина, который активирует развитие эритроцитов в костном мозге, что проявляется увеличением количества кроветворных клеток в нем (гиперплазией костного мозга). При талассемии гиперплазия костного мозга настолько выражена, что происходит деформация костей, в которых он располагается.Деформация костей при талассемии проявляется:
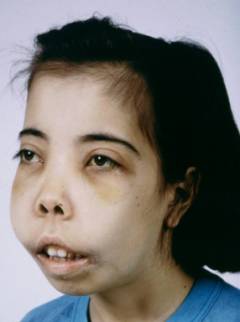
- увеличением костей черепа (голова непропорционально большая);
- уплощением переносицы;
- сужением глазных щелей (из-за чрезмерного разрастания формирующих их костей лицевого скелета);
- увеличением верхней челюсти и выступанием верхних зубов («лицо бурундука»);
- утолщением позвонков;
- расширением длинных трубчатых костей (сопровождается нарушением их структуры, что повышает риск переломов).
Симптомы избытка железа в организме
Перегрузка организма железом развивается как вследствие повышенного всасывания данного микроэлемента в кишечнике, так и в результате частых переливаний крови, применяемых в лечении талассемии. Результатом этого является повышение концентрации свободного железа в крови и его отложение практически во всех тканях организма.Наиболее опасными последствиями избытка железа в организме являются:
- Поражение гипофиза. Гипофиз – это железа, расположенная в основании черепа и выделяющая гормоны, контролирующие рост и развитие всего организма. Избыточное отложение железа в гипофизе может привести к нарушению его функции, результатом чего будет замедление роста, нарушение физического и умственного развития, нарушение полового созревания.
- Поражение сердца. Железо накапливается в сердечной мышце и разрушает мышечные клетки, которые впоследствии замещаются соединительной (рубцовой) тканью. Наличие рубцов нарушает нормальную работу сердца, что может проявляться различными заболеваниями (нарушениями ритма и частоты сердечных сокращений, сердечной недостаточностью, инфарктом миокарда и др.).
- Поражение печени. Разрушение клеток печени и разрастание в ней рубцовой (фиброзной) ткани характеризуется нарушением ее функций. Это может проявляться отсутствием аппетита, нарушением пищеварения, прогрессирующим снижением веса, частыми инфекционными заболеваниями и повышенной кровоточивостью (большинство факторов, отвечающих за свертывание крови, образуется в печени). При отсутствии соответствующего лечения возможно развитие цирроза (состояния, при котором большая часть печени замещается фиброзной тканью) и/или рака печени.
- Поражение почек. Отложение железа в почках приводит к нарушению их способности образовывать и выделять мочу, в результате чего в организме накапливается вода, а также множество конечных продуктов обмена веществ, которые в норме выводились с мочой. Наиболее тяжелым проявлением поражения почек является развитие почечной недостаточности, что часто требует лечения гемодиализом (аппаратом искусственной почки).
- Поражение кожи. Отложение железа в глубоких слоях кожи обуславливает изменение ее цвета и появление пятен темно-бронзового оттенка.
- Поражение легких. Характеризуется нарушением дыхательной функции органа, что еще больше усугубляет недостаток кислорода в организме.
Симптомы усиленного разрушения эритроцитов
Как было сказано ранее, разрушение эритроцитов при талассемии происходит как в костном мозге и в селезенке, так и непосредственно в сосудистом русле (более характерно для b-талассемии). В результате этих процессов в кровь выделяется большое количество продуктов распада эритроцитов, что обуславливает соответствующие клинические симптомы.Кроме того, усиленный распад эритроцитов еще более усугубляет дефицит кислорода на тканевом уровне, развивающийся из-за нарушения образования гемоглобина.
Проявлениями усиленного распада эритроцитов являются:
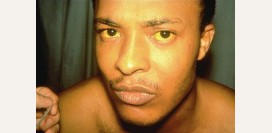
- желтушность кожных покровов;
- уратовый диатез;
- увеличение селезенки.
Как говорилось ранее, при разрушении эритроцита гемоглобин превращается в желтый пигмент – билирубин, который выделяется с желчью. При талассемии количество разрушаемых эритроцитов и попадающего при этом в кровоток билирубина настолько велико, что печень не успевает связывать и выводить его из организма. Результатом является повышение концентрации билирубина в крови (за счет несвязанной формы), а большие его количества, выделяемые с желчью, способствуют образованию камней в желчном пузыре.
Накапливаясь в кожных покровах и в слизистых оболочках (слизистой полости рта, конъюнктиве глаза), билирубин придает им характерный желтоватый оттенок. Наличие желтухи характерно для тяжелых форм заболевания и является неблагоприятным прогностическим признаком.
Увеличение селезенки (спленомегалия)
Селезенка является основным органом, обеспечивающим удаление из кровотока старых и поврежденных клеток крови. При талассемии основное число эритроцитов, образующихся в костном мозге и выделяющих в системный кровоток, имеют маленький размер и деформированную поверхность. Они не могут пройти через капилляры селезенки, в результате чего задерживаются и скапливаются в ней в больших количествах, обуславливая увеличение органа.
При длительной спленомегалии в селезенке начинают задерживаться не только деформированные эритроциты, но и другие, нормальные клетки крови (тромбоциты, лейкоциты). Они не могут пройти через капилляры органа, так как те полностью заполнены и перекрыты эритроцитами. Результатом этого процесса является развитие гиперспленизма – патологического процесса, характеризующегося разрушением нормальных клеток крови в увеличенной селезенке.
Уратовый диатез
Одним из веществ, выделяемых в кровоток в процессе разрушения клеток крови, является пурин. Он входит в состав нуклеиновых кислот - ДНК (дезоксирибонуклеиновой кислоты) и РНК (рибонуклеиновой кислоты), являющихся частью генетического аппарата клеток. Попавший в кровь пурин переносится в печень, где превращается в мочевую кислоту.
При повышении концентрации мочевой кислоты и ее солей (уратов) в крови, они могут образовывать кристаллические соединения, оседающие в различных тканях организма, вызывая их повреждение.
Накопление мочевой кислоты и ее солей может проявляться:
- Повреждением суставов. В результате отложения солей мочевой кислоты на суставных поверхностях костей происходит их деформация, что проявляется болями при движениях. При длительном течении заболевания развивается деформация суставных хрящей и ограничение объема движений в пораженных суставах.
- Поражением почек. Ураты накапливаются в почечной ткани и разрушают ее, что может привести к почечной недостаточности.
- Образованием уратных камней. Кристаллы солей мочевой кислоты могут накапливаться и формировать камни в почках либо в мочевом пузыре. Клинически это проявляется болями в поясничной области, затрудненным и болезненным мочеиспусканием, а также склонностью к инфекциям мочеполовых органов.
Диагностика талассемии
 Диагностикой и лечением талассемии занимается врач-гематолог, который, при необходимости, может привлекать специалистов из других областей медицины.
Диагностикой и лечением талассемии занимается врач-гематолог, который, при необходимости, может привлекать специалистов из других областей медицины.Основными методами, применяемыми в процессе диагностики талассемии, являются:
- общий анализ крови;
- биохимический анализ крови;
- дополнительные лабораторные исследования;
- рентгенологическое исследование;
- ультразвуковое исследование;
- пункция костного мозга;
- полимеразная цепная реакция (ПЦР).
Общий анализ крови
Самый простой, быстрый и безопасный метод, позволяющий выявить отклонения в клеточном составе периферической крови.Процедура забора крови
Кровь берут утром, натощак. Забор крови для анализа производит медицинская сестра. С целью предотвращения инфицирования кожу кончика пальца (чаще безымянного на левой руке) обрабатывают ватным тампоном, смоченным в 70% спирте, после чего специальной одноразовой игрой делают прокол на глубину 2 – 4 миллиметра. Первая капля удаляется ватным тампоном, после чего производится забор нескольких миллилитров крови.
Исследование крови в лаборатории
Часть полученной крови переносится на предметное стекло и окрашивается специальным красителем, после чего исследуется под микроскопом. Определяется количество эритроцитов (и других клеток крови), их форма, размеры, окраска.
Другим вариантом является помещение исследуемого материала в специальный аппарат – гематологический анализатор, в котором автоматически производится количественный подсчет всех клеточных элементов крови. Данный метод более точно определяет количество клеток крови, но не дает информации об их форме и строении.
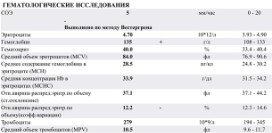
Изменения общего анализа крови при талассемии
| Показатель | Что обозначает | Норма | Изменения при талассемии |
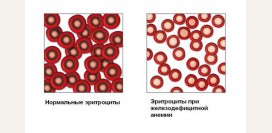
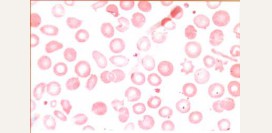
| Форма эритроцитов | Образующиеся при талассемии «лишние» цепи глобина не используются в синтезе гемоглобина, а скапливаются в центре клетки, что при исследовании в световом микроскопе придает эритроциту характерный внешний вид мишени. | Эритроциты однородно красного цвета, круглые, все одинакового размера. | Эритроциты овальной или округлой формы, представляющие собой светлые клетки с темным пятном в центре (мишеневидные эритроциты). |
| Размер эритроцитов | В результате нарушения образования гемоглобина развивается микроцитоз, характеризующийся образованием эритроцитов маленького диаметра. | 7,5 – 8,3 мкм. | 3 – 6 мкм. |
| Средний объем эритроцита (MCV) | Данный показатель вычисляется гематологическим анализатором посредством деления суммы объемов всех клеточных элементов на количество эритроцитов. Дает более точную информацию, чем простое определение размеров эритроцитов при исследовании под микроскопом. У детей и у пожилых людей средний объем эритроцитов может быть несколько повышен, что не является отклонением от нормы. | 75 – 100 кубических микрометров (мкм3). | Менее 70 мкм3 |
| Количество эритроцитов | При талассемии образуется большое количество маленьких эритроцитов, однако большинство из них очень быстро разрушается в селезенке, следствием чего является снижение общего числа данных клеток в крови. | Мужчины (М): 4,0 – 5,0 х 1012/л. | Менее 4,0 х 1012/л. |
| Женщины (Ж): 3,5 – 4,7 х 1012/л. | Менее 3,5 х 1012/л. | ||
| Общее количество гемоглобина | При талассемии синтез гемоглобина нарушен в различной степени (в зависимости от формы заболевания), в результате чего общее его количество в периферической крови снижено. | М: 130 – 170 г/л. | В зависимости от формы заболевания может быть нормальным или сниженным, вплоть до 10 г/л. |
| Ж: 120 – 150 г/л. | |||
| Средняя концентрация гемоглобина в эритроцитах (MCHC) | Высчитывается гематологическим анализатором и дает более точные данные о содержании гемоглобина именно в эритроцитах, а не в общем объеме крови. Вычисляется путем деления общего гемоглобина на показатель гематокрита. | 320 – 360 г/л. | Менее 300 г/л. |
| Количество тромбоцитов | При длительном течении заболевания может развиваться явление гиперспленизма, для которого характерно снижение количества всех клеток крови, в том числе и тромбоцитов. | 180 – 320 х 109/л. | Нормальное или сниженное. |
| Количество лейкоцитов | При талассемии отмечается склонность к частым инфекционным заболеваниям, что характеризуется повышением концентрации лейкоцитов. Однако при развитии гиперспленизма их количество в крови может уменьшаться, поэтому при оценке данного лабораторного показателя следует учитывать общее состояние пациента. | 4,0 – 9,0 х 109/л. | Варьирует в зависимости тяжести талассемии и общего состояния пациента. |
| Количество ретикулоцитов | Талассемия характеризуется усиленным процессом кроветворения в костном мозге, в результате чего в кровоток выделяется большое количество молодых форм эритроцитов. | М: 0,24 – 1,7%. | 2,5 – 4% и более. |
| Ж: 0,12 – 2,05%. | 3 – 5% и более. | ||
| Гематокрит | Данный показатель отображает отношение общего объема клеточных элементов крови к объему плазмы. Так как эритроциты являются основными клеточными элементами крови, снижение их количества и размеров при талассемии отразится на значении гематокрита. | М: 42 – 50%. | менее 32%. |
| Ж: 38 – 47%. | менее 38%. | ||
| Цветовой показатель | Отображает содержание гемоглобина в эритроцитах. При талассемии глобиновые цепи сконцентрированы в центре красных клеток крови, а количество нормального гемоглобина уменьшено, в результате чего цветовой показатель будет снижен. | 0,85 – 1,05. | 0,5 и ниже. |
| Скорость оседания эритроцитов (СОЭ) | В сосудистом русле эритроциты находятся в «подвешенном» состоянии в плазме крови. Если поместить кровь в пробирку и добавить туда антикоагулянт (вещество, предотвращающее процессы свертывания крови), то через некоторое время кровь разделится на два слоя - более тяжелые эритроциты осядут на дно пробирки, а более легкая плазма останется на поверхности. СОЭ определяется отрицательными зарядами на поверхности мембран эритроцитов, которые отталкиваются друг от друга, препятствуя оседанию клеток. При талассемии снижено как общее количество эритроцитов, так и их размеры, в результате чего СОЭ будет значительно увеличенной. | М: 3 – 10 мм/час. | более 10 мм/час. |
| Ж: 5 – 15 мм/час. | более 15 мм/час. |
Биохимический анализ крови
Данное исследование подразумевает определение наличия и концентрации определенных веществ в крови. Термин «биохимический анализ крови» включает несколько тысяч показателей, одновременная оценка которых невозможна и нецелесообразна. При каждом конкретном заболевании определяются лишь некоторые биохимические показатели, изменение которых может подтвердить или опровергнуть диагноз, а также дать врачу информацию о функционировании внутренних органов и состоянии обмена веществ в организме.За 24 часа до взятия крови необходимо исключить:
- выраженную физическую активность;
- прием большого количества жирной пищи;
- прием некоторых медикаментов (по возможности);
- употребление алкоголя и/или наркотических препаратов;
- курение.
Забор крови для биохимического анализа производит медицинская сестра. Обычно кровь берут из поверхностной вены в локтевой области, однако при определенных обстоятельствах (при ожирении, когда невозможно определить расположение вены) кровь могут брать из вены тыльной поверхности кисти.
Перед началом процедуры руку пациента перевязывают резиновым жгутом в области плеча (нарушается отток крови, вены руки переполняются кровью и становятся более заметными, что облегчает определение их расположения).
Предварительно обработав место предполагаемого укола смоченным в спирте ватным тампоном, медсестра вводит в вену иглу, к которой присоединен пустой шприц. Игла должна вводиться по направлению к телу пациента, что соответствует направлению тока крови в вене (это предотвращает образование тромбов после процедуры).
Вводя иглу в вену, медсестра постоянно оттягивает поршень шприца. Когда игла оказывается в вене (о чем свидетельствует появление в шприце крови темно-вишневого цвета), с плеча пациента снимается жгут и в шприц набирается несколько миллилитров крови, после чего к месту укола прижимается ватный шарик со спиртом, и игла извлекается. Кровь переносится в пробирку и отправляется в лабораторию на анализ. Пациента просят посидеть в коридоре в течение 15 – 20 минут во избежание появления осложнений (головокружения, потери сознания).
Биохимические показатели, определяемые при талассемии
| Показатель | Что обозначает | Норма | Изменения при талассемии |
| Уровень билирубина (общая фракция) | Общее количество билирубина в крови определяется путем сложения количества несвязанной и связанной форм. Данный показатель может быть повышен при усиленном распаде эритроцитов либо при заболеваниях печени и желчевыводящей системы, поэтому его определение носит ориентировочный характер и всегда должно сопровождаться определением отдельных фракций билирубина. | 0,5 – 20,5 мкмоль/л. | Чаще повышен, но может быть в пределах нормы. |
| Несвязанный билирубин | Данная фракция билирубина увеличивается при массивном разрушении эритроцитов в селезенке и в сосудистом русле, а также их предшественников (преимущественно эритробластов) в красном костном мозге. | 4,5 – 17,1 мкмоль/л. | Всегда повышен, может достигать нескольких сотен микромоль в 1 литре крови. |
| Уровень сывороточного железа | Как упоминалось ранее, при талассемии количество железа в крови повышается за счет усиления процессов его всасывания в кишечнике, а также в результате переливания больших объемов донорской крови. | М: 17,9 – 22,5 мкмоль/л. | Повышен при тяжелых формах заболевания, особенно в сочетании с увеличением селезенки и печени. |
| Ж: 14,3 – 17,9 мкмоль/л. | |||
| Уровень аланинаминотрансферазы (АлАТ) и аспартатаминотрансферазы (АсАТ) | Данные вещества находятся в клетках печени (гепатоцитах) в больших количествах. Увеличение их уровня в крови свидетельствует о разрушении гепатоцитов и выделении данных ферментов в кровь. Это может быть обусловлено развитием очагов кроветворения в печени либо токсическим действием свободного железа. | М: до 41 Ед/л. | При длительном течении заболевания может увеличиваться в десятки раз (в зависимости от степени поражения ткани печени). |
| Ж: до 31 Ед/л. | |||
| Уровень мочевой кислоты | Повышение данного показателя свидетельствует об усиленном процессе распада клеток крови в селезенке. | 2,5 – 8,3 ммоль/л. | Может повышаться в несколько раз, особенно при развитии гиперспленизма. |
Дополнительные лабораторные исследования
Кроме общего и биохимического анализа часто проводятся другие лабораторные исследования крови, которые помогают определить выраженность талассемии и степень нарушения кроветворной функции костного мозга.В диагностике талассемии применяются:
- определение общей железосвязывающей способности плазмы;
- определение концентрации ферритина в сыворотке крови;
- определение уровня эритропоэтина.
Метод основан на способности трансферрина связывать и транспортировать железо в нетоксичной форме. В нормальных условиях лишь часть активных центров данного белка связана с железом, остальные же остаются свободными. С помощью этого механизма регулируется концентрация свободного железа - при ее увеличении железо связывается со свободными активными центрами трансферрина, превращаясь в нетоксичную форму.
Общая железосвязывающая способность плазмы отображает количество свободных активных центров трансферрина в крови. Кровь берется из вены с соблюдением всех правил, описанных ранее. Суть метода довольно проста - в пробирку с кровью добавляют заранее известное избыточное количество свободного железа. Часть железа связывается со свободными активными центрами трансферрина, остальное удаляется и с помощью специальных приборов определяется его количество. На основании полученных данных делаются выводы об ОЖСС.
Нормальные значения ОЖСС находятся в интервале от 45 до 77 мкмоль/л. При талассемии количество свободного железа в крови значительно превышает норму. Все активные центры трансферрина находятся в связанном состоянии и практически лишены способности связывать железо, в результате чего ОЖСС снижается.
Определение концентрации ферритина в сыворотке крови
Исследованиями последних лет установлено, что количество ферритина в плазме находится в прямой зависимости от количества свободного железа в организме - при его увеличении увеличивается и концентрация ферритина.
На основании описанного механизма разработано множество методов определения концентрации данного белка в крови. Одним из наиболее часто используемых является радиоиммунный анализ. Кровь для данного исследования берется из вены, утром, натощак (правила забора описаны выше).
Суть метода заключается в следующем - на определенном твердом носителе фиксируется специальное вещество (антитело), которое способно избирательно связываться с ферритином. К нему добавляется образец исследуемой крови, при этом весь ферритин связывается с данным веществом, образуя прочное соединение.
Следующим этапом является добавление в раствор других специфических антител, к которым прикреплена радиоактивная метка (чаще используется атом йода). Свободные антитела связываются с ферритином и при удалении раствора задерживаются на твердом носителе.
Последним этапом является исследование в специальном гамма-счетчике, позволяющее определить количество радиоактивного йода на прикрепленных к ферритину антителах. На основании полученных данных делают выводы о концентрации ферритина в крови.
Норма ферритина в сыворотке крови зависит от пола и составляет:
- у мужчин – 20 – 250 мкг/л;
- у женщин – 10 – 125 мкг/л.
Определение уровня эритропоэтина
Суть метода заключается в определении количества эритропоэтина в плазме крови. С данной целью также можно применять радиоиммунный анализ. Техника и правила выполнения такие же, только вместо антител к ферритину используются специфические антитела к эритропоэтину.
Нормальная концентрация эритропоэтина в крови составляет 10 – 30 мМЕ/мл (международных миллиединиц в 1 миллилитре). При талассемии данный показатель увеличен в несколько раз, что обусловлено избыточной продукцией эритропоэтина почками.
Рентгенологическое исследование
Простой метод исследования, позволяющий получить теневое изображение костей и внутренних органов человека. Суть метода заключается в способности рентгеновских лучей проходить через ткани организма и частично поглощаться ими. В результате этого процесса на специальной пленке образуются теневые проекции органов исследуемой области.Различные органы и ткани поглощают рентгеновские лучи с разной интенсивностью, в результате чего их теневые отображения на рентгеновской пленке будут более или менее четкими. Максимальной поглощающей способностью в организме человека обладает костная ткань, которая характеризуется наиболее светлыми участками на рентгеновских снимках. Воздух практически не поглощает рентгеновские лучи и определяется как наиболее темный участок на снимке.
При рентгенологическом исследовании больных талассемией можно выявить:
- Деформацию костей черепа. Отмечается их расширение и снижение плотности на рентгенограмме, что обусловлено разрастанием костномозгового вещества и уменьшением количества костной ткани.
- Деформацию длинных трубчатых костей. Проявляется уменьшением плотности костей, их утолщением и искривлением.
- Увеличение размеров селезенки и печени.
Противопоказаниями к выполнению рентгенологического исследования являются:
- ранний детский возраст;
- опухолевые процессы в организме;
- наличие металлических имплантатов в исследуемой области.
Ультразвуковое исследование
Данный метод абсолютно безопасен и безвреден, с его помощью можно быстро и точно определить размеры и форму внутренних органов.Метод основан на способности ультразвуковых волн (частота которых превышает 20 000 герц) проходить через ткани организма и частично отражаться ими. Максимальная степень отражения ультразвука определяется на границе двух различных сред (например, воздуха и жидкости, воздуха и ткани органа, ткани органа и кости). Таким образом возможно получить изображение внутренних тканей и органов, изучить их структуру, плотность и консистенцию.
Современные аппараты УЗИ довольно компактны и просты в применении, поэтому проведение исследования возможно прямо в кабинете врача. Пациент ложится на кушетку и оголяет исследуемую часть тела. На поверхность кожи наносится специальный гель, который заполняет микротрещины кожных покровов (содержащийся в них воздух может создать помехи при исследовании), после чего к коже прикладывается датчик, излучающий ультразвук.
Отраженные ультразвуковые волны регистрируются специальным приемником, и после компьютерной обработки на экране появляется изображение исследуемого органа или области.
При диагностике талассемии проводится:
- УЗИ печени. Печень увеличена в размерах, повышенной плотности, неоднородной консистенции, с неровными краями. Могут отмечаться более плотные участки, соответствующие разрастанию рубцовой ткани.
- УЗИ селезенки. Селезенка значительно увеличена, неоднородной консистенции и повышенной плотности, переполнена кровью.
- УЗИ почек и мочевого пузыря. Позволяет выявить наличие камней, образующихся в результате повышенного выделения мочевой кислоты с мочой.
Пункция костного мозга
Данный метод позволяет детально изучить клеточный состав костного мозга, на основании которого можно сделать выводы о выраженности и характере процессов кроветворения.Забор материала для исследования проводится в стерильных условиях стерильными инструментами. Чаще всего костный мозг берут из грудины, однако возможна пункция и других плоских костей (костей таза, позвонков).
После обработки места пункции раствором 70% спирта шприцом со специальной иглой прокалывают надкостницу и верхнюю часть кости. Иглу продвигают вглубь на 1 – 1,5 см, после чего производится забор 0,5 – 1 мл вещества костного мозга. Иглу извлекают, место пункции прикрывается стерильным пластырем. Полученный материал отправляется в лабораторию, где производится его окрашивание специальными красителями и исследование под микроскопом.
При исследовании пунктата костного мозга больных талассемией определяется выраженное увеличение количества клеток, в основном предшественников эритроцитов. Они имеют характерное строение и размер (маленькие светлые клетки со скоплением гемоглобина в центре).
Полимеразная цепная реакция
С помощью данного метода можно выявить мутантный ген и хромосому, в которой он расположен, что позволяет подтвердить или опровергнуть диагноз талассемии в 99,9% случаев.Принцип метода заключается в образовании большого количества копий определенного гена с последующим его изучением. Для исследования необходимо небольшое количество биологического материала, содержащего клетки (кровь, слюна, моча и т. д.). Исследуемый материал помещается в пробирку, и к нему добавляется набор специальных ферментов и реактивов, которые активируют процесс удвоения строго определенного гена на определенной хромосоме, и только в том случае, если этот ген присутствует в генетическом аппарате клетки.
Другими словами, для того чтобы получить копии гена, кодирующего, например, образование а-цепи глобина, необходимо, чтобы он присутствовал в 16 хромосоме и не был деформирован. В этом случае специальные вещества распознают этот ген, присоединяться и копируют его, после чего процесс повторится множество раз. Если же данного гена в хромосоме нет (при а-талассемии), никаких реакций не происходит.
По такому же принципу определяется наличие или отсутствие всех генов, отвечающих за образование различных цепей глобина. Это помогает установить форму талассемии и определить вероятность передачи заболевания потомкам.
Устранение осложнений талассемии
 К сожалению, на современном этапе развития медицины не существует лекарства, способного избавить человека от этого недуга. Большие надежды подает метод пересадки стволовых кроветворных клеток (пересадки костного мозга), однако его выполнение сопряжено с множеством трудностей и не всегда возможно. Вот почему целью лечения в большинстве случаев является устранение симптомов заболевания и предупреждение развития осложнений.
К сожалению, на современном этапе развития медицины не существует лекарства, способного избавить человека от этого недуга. Большие надежды подает метод пересадки стволовых кроветворных клеток (пересадки костного мозга), однако его выполнение сопряжено с множеством трудностей и не всегда возможно. Вот почему целью лечения в большинстве случаев является устранение симптомов заболевания и предупреждение развития осложнений.Легкие формы талассемии часто не нуждаются в лечении. Таким пациентам рекомендуется профилактическая сдача общего анализа крови раз в полгода. При более тяжелых формах лечение следует начинать как можно раньше, так как недостаток кислорода в организме может привести к развитию необратимых изменений во внутренних органах.
Основными направлениями в лечении талассемии являются:
- повышение уровня эритроцитов и гемоглобина в крови;
- устранение переизбытка железа;
- снижение уратового диатеза;
- хирургическое удаление селезенки;
- пересадка костного мозга.
Повышение уровня эритроцитов и гемоглобина в крови
При тяжелых формах талассемии количество нормального гемоглобина может снижаться с первых дней жизни ребенка, что требует незамедлительного начала лечения.Единственным эффективным способом повышения количества эритроцитов и гемоглобина в крови является переливание донорской крови. Целевой уровень гемоглобина при этом составляет 100 – 120 г/л.
Показаниями к переливанию крови являются:
- подтвержденный (лабораторно) диагноз талассемии;
- снижение общего гемоглобина ниже 70 г/л;
- задержка роста;
- деформация костей черепа;
- определение очагов экстрамедуллярного кроветворения.
Возможными побочными реакциями при переливании крови являются:
- повышение температуры тела;
- аллергические реакции;
- массивное разрушение эритроцитов (в результате переливания несовместимой крови);
- инфицирование реципиента (больного, которому переливается кровь).
Методы повышения уровня эритроцитов и гемоглобина
| Название методики | Механизм лечебного действия | Способ применения | Оценка эффективности лечения |
| Переливание цельной донорской крови | Донорская кровь содержит все клетки крови (эритроциты, тромбоциты, лейкоциты и лимфоциты). Эффектами переливания донорской крови являются:
| Цельная донорская кровь назначается довольно редко, ввиду множества побочных реакций. Единственным обоснованным показанием является развитие гиперспленизма с уменьшением количества всех клеток крови. Переливание крови производится 1 – 3 раза в месяц, в зависимости от формы и тяжести заболевания. За 1 раз может быть перелито 500 и более миллилитров крови. | Критериями эффективности лечения являются:
|
| Переливание эритроцитарной массы | Пациенту переливаются чистые (отмытые) эритроциты. Лечебные эффекты такие же, как при переливании цельной крови, однако данный метод характеризуется значительно меньшим количеством осложнений, что обусловлено меньшим количеством чужеродных клеток, поступающих в организм. | В зависимости от показателей гемоглобина и клинической картины заболевания эритроциты переливают от 1 до 3 – 4 раз в месяц. Длительность лечения – пожизненная. | Критерии эффективности лечения такие же, как при переливании препаратов цельной крови. |
Устранение переизбытка железа в организме
Лечение перегрузки железом следует начинать одновременно с переливанием крови, чтобы предотвратить накопление железа в тканях (в этом случае выведение излишков железа из организма будет более длительным, а поражения органов более выраженными). Медикаментозное лечение избытка железа в организме
| Название препарата | Механизм лечебного действия | Способ применения и дозы | Оценка эффективности лечения |
| Десферал (Дефероксамин) | Данный препарат обладает способностью связывать как свободное, так и входящее в состав ферритина и трансферрина железо. Образующиеся при этом комплексы нетоксичны и быстро выводятся из организма. | Назначается при повышении ферритина в сыворотке выше 1000 мкг/л. Препарат вводится внутривенно, капельно, в дозе 20 – 40 мг/кг/день, минимум 5 дней в неделю. Длительность лечения – пожизненная. | Критериями эффективности лечения являются:
|
| Эксиджад | Механизм действия такой же, как у десферала, однако данный препарат более избирательно фиксирует железо, практически не влияя на обмен других микроэлементов крови. | Принимать внутрь, 1 раз в сутки (желательно в одно и то же время), за 30 минут до еды. Начальная доза 10 мг/кг, при необходимости может быть повышена до 30 мг/кг. Длительность лечения – не менее 1 года. | Критерии эффективности лечения такие же, как при приеме десферала. |
| Витамин С | Способствует выведению железа из организма. | Принимать внутрь, 2 – 3 раза в день. Рекомендуемая доза – 1 – 3 мг/кг/сутки. Не рекомендуется назначать одновременно с десфералом. | Критерии эффективности лечения такие же, как при приеме десферала. |
Снижение уратового диатеза
С целью снижения количества мочевой кислоты и ее солей в крови назначаются определенные медикаменты, снижающие скорость образования мочевой кислоты, либо способствующие ускоренному выведению ее из организма. Медикаментозное лечение уратового диатеза
| Название медикамента | Механизм лечебного действия | Способ применения и дозы | Оценка эффективности лечения |
| Аллопуринол | Противоподагрический препарат, применяемый для уменьшения количества уратов в крови. Основными эффектами являются:
| Внутрь, 3 раза в день, после еды. Начальная доза 70 – 130 мг. При необходимости доза может быть увеличена до 200 мг. Лечение длительное. | Критериями эффективности лечения являются:
|
| Бенемид | Урикозурический препарат, повышающий выделение мочевой кислоты с мочой. Кроме того повышает количество выделяемой в сутки мочи, что препятствует образованию камней в почках и мочевом пузыре. | Внутрь, после еды. Начальная доза – 0,5 г/сутки. Постепенно доза увеличивается, пока не нормализуется концентрация мочевой кислоты в крови (максимум 3 г/сутки). Лечение пожизненное. | Критериями эффективности лечения являются:
|
Хирургическое удаление селезенки
При тяжелых формах талассемии селезенка может увеличиваться в несколько раз, обуславливая развитие множества осложнений. В таких случаях возможно удаление органа хирургическим путем (спленэктомия), что устраняет или снижает выраженность некоторых проявлений заболевания.Показаниями к хирургическому удалению селезенки при талассемии являются:
- Развитие гиперспленизма.
- Выраженное разрушение эритроцитов в селезенке, требующее частых переливаний эритроцитарной массы.
- Значительное увеличение мочевой кислоты и ее солей в крови, не поддающееся медикаментозной терапии.
- Выраженная желтуха, обусловленная выделением большого количества билирубина из разрушаемых эритроцитов.
Операция выполняется под общим наркозом. Доступ чаще всего лапаротомический - производится разрез в области живота, сосуды селезенки вначале перевязываются, а затем перерезаются, и орган удаляется. Место разреза ушивают стерильными нитками и накладывают стерильную повязку, которую меняют каждый день. После операции рекомендуется исключить физические нагрузки в течение как минимум одного месяца.
Пересадка костного мозга
На сегодняшний день это единственный метод, способный полностью излечить больного талассемией. Суть метода заключается в полном разрушении всего костного мозга пациента и введении в освободившиеся костные полости донорского костного мозга. Если процедура увенчается успехом и донорский костный мозг приживется в организме реципиента, это обеспечит нормальный синтез глобиновых цепей, что устранит центральное звено в развитии талассемии.Проведение пересадки костного мозга включает множество этапов, основными из которых являются:
- Поиск донора. Является наиболее важным и трудоемким процессом, так как костный мозг донора должен максимально соответствовать костному мозгу реципиента по множеству критериев. Рекомендуется, чтобы донор и реципиент не состоял в близком родстве, однако если другого варианте нет – перед пересадкой костного мозга проводится его генетическое исследование (ПЦР), с целью выявления малых форм талассемии, не проявляющихся клинически.
- Подготовка донора и забор костного мозга. После проведения многочисленных тестов на совместимость донор госпитализируется. В стерильной операционной под общим наркозом специальной иглой, подсоединенной к шприцу, прокалываются кости таза и бедренные кости, из которых производится забор определенного количества костного мозга. Общий объем полученного материала не должен превышать 2000 мл. На следующий день донор может быть выписан из больницы.
- Подготовка реципиента. Чтобы донорский костный мозг прижился, необходимо в первую очередь полностью разрушить собственный костный мозг. С этой целью в течение нескольких дней перед выполнением пересадки реципиент получает максимальные дозы сильнодействующих цитостатических препаратов (бусульфана, циклофосфана), что в идеале должно привести к гибели абсолютно всех кроветворных клеток организма (включая экстрамедуллярные очаги кроветворения в селезенке и печени). Иногда с этой же целью может применяться радиационное облучение тела реципиента.
- Введение костного мозга реципиенту. Введение костного мозга производится через катетер – специальную трубку, установленную в центральную вену реципиента (чаще подключичную). Сам процесс довольно прост и мало чем отличается от обычного переливания крови.
- Наблюдение за реципиентом. Первые 3 – 4 недели пациенту требуются постоянные переливания всех компонентов крови и прием больших доз антибиотиков, так как предшествующая химиотерапия уничтожила почти все защитные функции организма. Если костный мозг приживется, то через несколько месяцев уровень гемоглобина и всех клеточных элементов в крови пациента начнет повышаться. При нормализации лабораторных данных пациент выписывается из больницы (в среднем через 6 – 8 недель после пересадки). В течение первого года необходим ежемесячный контроль показателей крови, а в дальнейшем сдача общего анализа крови производится раз в полгода.